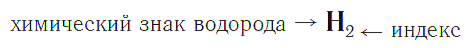что означает молекулярная формула
Урок 5. Химическая формула
В уроке 5 «Химическая формула» из курса «Химия для чайников» дадим определение химическим формулам и их индексам, а также выясним различия химических формул веществ молекулярного и немолекулярного строения. Напоминаю, что в прошлом уроке «Сложные вещества» мы дали определение химическим соединениям, рассмотрели различия органических и неорганических соединений, а также выяснили, что означает качественный и количественный состав.
Состав любого вещества выражается в виде химической формулы.
Качественный состав показывается с помощью знаков (символов) химических элементов, а количественный — с помощью индексов, которые записываются справа и чуть ниже знаков химических элементов.
Индекс — число атомов данного химического элемента в формуле вещества.
Например, химическая формула простого вещества водорода записывается так:
Химические формулы веществ молекулярного строения
Формулы двухатомных молекул: кислорода — О2 («о-два»), хлора — Сl2 («хлор-два»), азота — N2 («эн-два»). Трехатомная молекула озона и восьмиатомная молекула серы обозначаются формулами О3 («о-три») и S8 («эс-восемь»).
Формулы молекул сложных веществ также отображают их качественный и количественный состав. Например, формула воды, как вы уже, наверное, хорошо знаете, Н2О («аш-два-о»), метана — СН4 («це-аш-четыре»), а аммиака — NH3 («эн-аш-три»). Точно так же читаются формулы любых сложных веществ. Например, формула серной кислоты — H2SO4 («аш-два-эс-о-четыре»), а глюкозы — C6H12O6 («це-шесть-аш-двенадцать-о-шесть»).
Химические формулы веществ молекулярного строения (их называют молекулярными формулами) показывают состав элементарных частей, т. е. условных «кирпичиков», из которых состоят эти вещества. Такими элементарными составными частями (элементарными структурными единицами, или просто структурными единицами) в данном случае являются молекулы.
Химические формулы веществ немолекулярного строения
А если вещество имеет немолекулярное строение? Химические формулы простых веществ такого типа (например, металлов) записывают просто знаками соответствующих элементов без индексов (или, вернее, с индексом, равным единице, которая не записывается). Так, формула простого вещества железа — Fe, меди — Cu, алюминия — Al.
Состав сложных веществ немолекулярного строения выражают с помощью формул, которые показывают простейшее соотношение чисел атомов разных химических элементов в этих веществах. Такие формулы называются простейшими. Например, простейшая формула кварца — главной составной части речного песка — SiO2. Она показывает, что в кристалле кварца на один атом кремния приходятся два атома кислорода, т. е. простейшее соотношение чисел атомов кремния и кислорода в этом веществе равно 1:2. Простейшая формула Al2O3 показывает, что в этом соединении простейшее соотношение между числами атомов алюминия и кислорода равно 2:3.
Группа атомов, состав которой соответствует простейшей формуле вещества немолекулярного строения, называется его формульной единицей.
Формульная единица, поваренной соли NaCl («натрий-хлор») — группа из одного атома натрия и одного атома хлора. Формульная единица мела CaCO3 («кальций-це-о-три») — группа из одного атома кальция, одного атома углерода и трех атомов кислорода.
Формулы более сложных соединений немолекулярного строения читаются аналогично. Дополнительно указывается только число групп атомов, заключенных в круглые скобки: Al2(SO4)3 («алюминий-два-эс-о-четыре-трижды»), Mg(NO3)2 («магний-эн-о-три-дважды») и т. д.
Таким образом, структурными единицами веществ молекулярного строения являются молекулы. Структурными единицами веществ немолекулярного строения являются их формульные единицы.
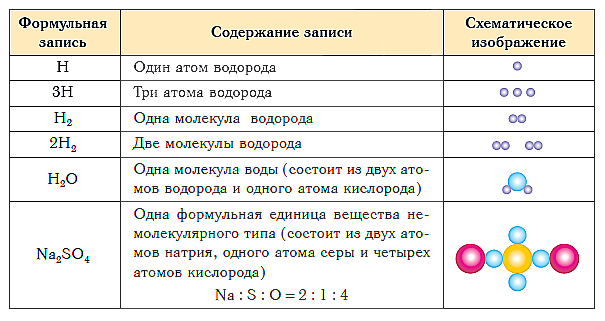
В таблице ниже показаны формульная запись и схематическое изображение состава веществ различного типа.
Краткие выводы урока:
Надеюсь урок 5 «Химическая формула» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Молекулы. Химические формулы. Молекулярные массы
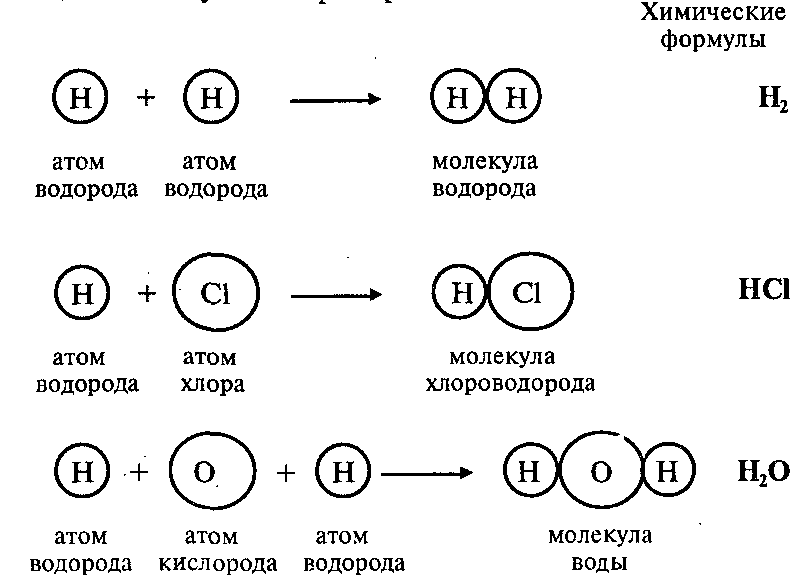
Атомы могут соединяться друг с другом. В результате этого соединения обычно образуются более сложные частицы – молекулы. Например:
Эти примеры показывают, что соединяться друг с другом могут атомы одного элемента и атомы разных элементов. Число атомов, которые соединяются друг с другом, может быть различным.
Состав любой молекулы можно выразить химической формулой.
Так, молекула водорода имеет формулу Н2. Число «2» в этой формуле показывает число атомов водорода в молекуле водорода.
Числа в химических формулах, которые показывают, сколько атомов данного элемента входит в состав молекулы, называются индексами.
Молекула хлороводорода имеет формулу НCl, так как она состоит из одного атома водорода и одного атома хлора. Молекула воды имеет формулу Н2O. Эта формула показывает, что молекула воды состоит из двух атомов водорода и одного атома кислорода.
Молекула серной кислоты состоит из двух атомов водорода Н, одного атома серы S и четырех атомов кислорода О. Значит, формула молекулы серной кислоты — H2SO4.
Существуют молекулы, в состав которых входит несколько одинаковых групп атомов. В формулах таких молекул эти группы атомов заключают в скобки, а индекс за скобками показывает число этих групп в молекуле. Например, формула Cu(NO3)2 показывает, что эта молекула состоит из одного атома меди и двух групп атомов NО3, т. е. двух атомов азота и шести атомов кислорода.
Таким образом, химические формулы доказывают качественный и количественный состав молекулы (из атомов каких элементов состоит молекула и сколько этих атомов в молекуле).
Согласно закону постоянства состава (Ж. Пруст, Франция, 1808 г.): Каждое чистое вещество имеет постоянный качественный и количественный состав, который не зависит от способа получения вещества.
Так как вещество состоит из одинаковых молекул, то состав молекулы определяет состав всего вещества. Различия в химических свойствах веществ обусловлены различиями в составе и строении молекул, из которых состоят эти вещества. Поэтому можно сделать вывод:
Молекула — это наименьшая частица вещества, которая сохраняет его химические свойства.
Масса любой молекулы равна сумме масс образующих ее атомов. Если при расчете массы молекулы используются относительные атомные массы, то получается относительная молекулярная масса, которая обозначается символом Мr.
Например, относительная молекулярная масса воды Н2O равна:
Mr(H2О) = Ar(H) + Аr(Н) + Аr(О) = 2Аr(Н) + Аr(О) =2∙1+16=18;
относительная молекулярная масса сульфата железа (III) Fe2(SO4)3 равна: Mr[Fe2(SO4)3] = 2Ar(Fe) + 3Ar(S) + 12Ar(O) = 2∙56+3∙32+12∙16=400;
Относительная молекулярная масса вещества Мr — это число, которое показывает, во сколько раз абсолютная масса молекулы данного вещества больше 1/12 части абсолютной массы атома углерода С.
Например, относительная молекулярная масса воды Mr(H2О) = 18. Это значит, что масса молекулы воды в 18 раз больше 1/12 части массы атома углерода.
Относительные молекулярные массы, как и относительные атомные массы, являются величинами безразмерными.
По формуле вещества можно рассчитать массовую долю каждого химического элемента, который входит в состав вещества.
Массовая доля (ω) химического элемента в данном веществе равна отношению относительной атомной массы данного элемента, умноженной на число его атомов в молекуле, к относительной молекулярной массе вещества:
где ω(Х) — массовая доля элемента Х; Ar(X) — относительная атомная масса элемента Х; n — число атомов элемента Х в молекуле вещества; Мr — относительная молекулярная масса вещества.
Молекулярная формула
Что такое молекулярная формула
Современные символы химических элементов были введены в науку в 1813 году Я. Берцелиусом. По его предложению элементы обозначаются начальными буквами их латинских названий. Например, кислород (Oxygenium) обозначается буквой О, сера (Sulfur) – буквой S, водород (Hydrogenium) – буквой Н. В тех случаях, когда названия элементов начинаются с одной и той же буквы, к первой букве добавляется еще одна из последующих. Так, углерод (Carboneum) имеет символ С, кальций (Calcium) – Ca, медь (Cuprum) – Cu.
Химические символы – не только сокращенные названия элементов: они выражают и определенные их количества (или массы), т.е. каждый символ обозначает или один атом элемента, или один моль его атомов, или массу элемента, равную (или пропорциональную) молярной массе этого элемента. Например, С означает или один атом углерода, или один моль атомов углерода, или 12 единиц массы (обычно 12 г) углерода.
Молекулярная формула веществ
Формулы веществ также указывают не только состав вещества, но и его количество и массу. Каждая формула изображает или одну молекулу вещества, или один моль вещества, или массу вещества, равную (или пропорциональную) его молярной массе. Например, H2O обозначает или одну молекулу воды, или один моль воды, или 18 единиц массы (обычно (18 г) воды.
Простые вещества также обозначаются формулами, показывающими, из скольких атомов состоит молекула простого вещества: например, формула водорода H2. Если атомный состав молекулы простого вещества точно не известен или вещество состоит из молекул, содержащих различное число атомов, а также, если оно имеет не молекулярное, а атомное или металлическое строение, простое вещество обозначают символом элемента. Например, простое вещество фосфор обозначают формулой P, поскольку в зависимости от условий фосфор может состоять из молекул с различным числом атомов или иметь полимерное строение.
Формулу вещества устанавливают на основании результатов анализа. Например, согласно данным анализа глюкоза содержит 40% (масс.) углерода, 6,72% (масс.) водорода и 53,28% (масс.) кислорода. Следовательно, массы углерода, водорода и кислорода относятся друг к другу как 40:6,72:53,28. Обозначим искомую формулу глюкозы CxHyOz, где x, y и z – числа атомов углерода, водорода и кислорода в молекуле. Массы атомов этих элементов соответственно равны 12,01; 1,01 и 16,00 а.е.м. Поэтому в составе молекулы глюкозы находится 12,01х а.е.м. углерода, 1,01у а.е.м. водорода и 16,00zа.е.м. кислорода. Отношение этих масс равно 12,01х: 1,01у: 16,00z. Но это отношение мы уже нашли, исходя из данных анализа глюкозы. Следовательно:
12,01х: 1,01у: 16,00z = 40:6,72:53,28.
Согласно свойствам пропорции:
x: у: z = 40/12,01:6,72/1,01:53,28/16,00
или х: у: z = 3,33 : 6,65 : 3,33 = 1 : 2 : 1.
Следовательно, в молекуле глюкозы на один атом углерода приходится два атома водорода и один атом кислорода. Этому условию удовлетворяют формулы CH2O, C2H4O2, C3H6O3 и т.д. Первая из этих формул — CH2O — называется простейшей или эмпирической формулой; ей отвечает молекулярная масса 30,02. Для того, чтобы узнать истинную или молекулярную формулу, необходимо знать молекулярную массу данного вещества. Глюкоза при нагревании разрушается, не переходя в газ. Но ее молекулярную массу можно определить и другими методами: она равна 180. Из сопоставления этой молекулярной массы с молекулярной массой, отвечающей простейшей формуле, ясно, что глюкозе отвечает формула C6H12O6.
Таким образом, химическая формула – это изображение состава вещества с помощью символов химических элементов, числовых индексов и некоторых других знаков, а молекулярную формулу вещества можно получить, зная простейшую формулу вещества и его молекулярную массу.
Примеры решения задач
| Задание | При сжигании 8,4 г углеводорода получили 26,4 г углекислого газа и 10,8 г воды. Относительная плотность паров углеводорода по воздуху равна 42. Найдите молекулярную формулу углеводорода. |
| Решение | Значение молярной массы углеводорода можно определить при помощи его плотности по водороду: |
По массам углекислого газа и воды находим массы углерода и водорода. Однако, для начала рассчитаем их молярные массы. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr):
M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль;
M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль.
m (C) = 26,4×12/44 = 7,2 г.
m (H) = 10,8 × 2×1 / 18 = 1,2 г.
Обозначим количество моль элементов, входящих в состав соединения за «х» (углерод) и «у» (водород). Тогда, мольное отношение будет выглядеть следующим образом:
Следовательно, простейшая формула углеводорода имеет вид CH2и молярную массу 14 г/моль [M(CH2) = Ar(C) + 2×Ar(H) = 12+ 2×1 = 12 + 2 = 14 г/моль].
Чтобы найти истинную формулу оксида хлора найдем отношение полученных молярных масс:
Значит индексы атомов углерода и водорода должны быть в 6 раз выше, т.е. формула углеводорода будет иметь вид C6H12. Это гексен.
| Задание | При сгорании 2,3 г органического вещества, состоящего из углерода, водорода и кислорода, образовалось 4,4 г углекислого газа и 2,7 г воды. Плотность паров вещества по кислороду равна 1,44 г. Определите молекулярную формулу вещества. |
| Решение | Значение молярной массы углеводорода можно определить при помощи его плотности по кислороду: |
Msubstance = 32 × 1,44 = 46 г/моль.
По массам углекислого газа и воды находим массы углерода и водорода, а также кислорода (по разнице между массой вещества и атомов углерода и водорода в нем). Однако, для начала рассчитаем их молярные массы. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr):
M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль;
M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль.
m (C) = 4,4×12/ 44 = 1,2 г.
m (H) = 2,7 × 2×1 / 18 = 0,3 г.
m(O) = msubstance — m (C) — m (H) = 2,3 – 1,2 – 0,3 = 0,8 г.
Обозначим количество моль элементов, входящих в состав соединения за «х» (углерод), «у» (водород) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом:
x:y:z = m(C)/Ar(C) : m(H)/Ar(H) : m(O)/Ar(O);
x:y:z= 1,2/12 : 0,3/1: 0,8/16;
x:y:z= 0,1 : 0,3: 0,05 = 2 : 6 : 1.
Следовательно, простейшая формула органического соединения имеет вид C2H6O и молярную массу 46 г/моль [M(C2H6O) = 2×Ar(C) + 6×Ar(H) + Ar(O) = 2×12+ 6×1 + 16= 24 + 6 + 16 = 46 г/моль].
Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс:
Значит формула органического соединения будет иметь вид C2H6O.
Молекулярная формула: как получить, примеры и упражнения
Содержание:
В молекулярная формула Это представление молекулы соединения, в котором атомы всех элементов, присутствующих в соединении, и их количество обозначены их химическими символами. Каждый атом сопровождается нижним индексом.
Молекулярная формула имеет ограничение, которое не указывает ни на связи различных атомов молекулы, ни на их пространственное соотношение; как это делает структурная формула. В некоторых случаях он не конкретен, например: C6ЧАС12ИЛИ6 это молекулярная формула глюкозы, галактозы и фруктозы.
Молекулярная формула органических соединений записывается путем размещения сначала символа углерода (C), затем символа водорода (H), а затем оставшихся атомов. Например, молекулярная формула уксусной кислоты C2ЧАС4ИЛИ2.
Как получить молекулярную формулу
Получение молекулярной формулы соединения основано на предварительном установлении его минимальной или эмпирической формулы. По этой причине начальные этапы получения обеих формул являются общими.
Первый шаг
Обычно массу элементов химического соединения выражают в процентах. Затем необходимо выполнить простой расчет, чтобы преобразовать массовые проценты различных элементов в их массы, выраженные в граммах.
Второй шаг
Зная массу в граммах каждого из элементов и их атомную массу, относительное число каждого атома или число молей каждого атома можно получить, разделив массу каждого из различных элементов на их атомную массу.
Третий шаг
Разделите относительное количество все атомов, введите относительное количество меньшего значения. Значения минимальной доли должны быть целыми числами. В случае, если значение пропорции содержит десятичную дробь, необходимо внести поправку, чтобы эта десятичная дробь исчезла.
Коррекция заключается в умножении всех значений пропорции на число, которое возвращает все значения в целые числа. Например, если значение минимальной пропорции составляет 1,25, все значения необходимо умножить на четыре (4). Поскольку 1,25, умноженное на 4, равняется 5, целому числу.
Четвертый шаг
Все химические символы элементов соединения будут помещены с соответствующими индексами; то есть значение минимальной доли элемента.
Пятый шаг
Минимальная формула соединения может быть преобразована в его молекулярную формулу, получая соотношение между молекулярной массой соединения и массой его минимальной формулы (n). Это соотношение такое же, как между молекулярной формулой и формулой минимума.
n = молекулярная масса соединения / масса минимальной формулы
Чтобы получить молекулярную формулу, умножьте формулу минимума на n. Это означает, что каждый из нижних индексов формулы минимума необходимо умножить на n.
n = Молекулярный вес / Минимальный вес формулы
= Молекулярная формула / Минимальная формула
Молекулярная формула = nминимальная формула
Примеры молекулярных формул
Некоторые общие молекулярные формулы перечислены ниже:
-Гидроксид натрия (NaOH)
-Оксид хлорной кислоты (Cl2ИЛИ7)
Химическая формула – определение, виды и примеры
Определение химической формулы
Химическая формула представляет собой обозначение, используемое учеными, чтобы показать количество и тип атомов, присутствующих в молекула, используя атомарные символы и числовые индексы. Химическая формула представляет собой простое письменное представление существующей трехмерной молекулы. Химическая формула описывает вещество, вплоть до точных атомов, из которых оно состоит. Существует три основных типа химической формулы: эмпирическая формула, молекулярная формула и структурная формула.
Каждая из этих химических формул предоставляет немного различную информацию о составе вещества и подсказывает его трехмерную форму и то, как оно будет взаимодействовать с другими молекулами, атомами и ионами. В химической формуле буквы представляют атомный символ каждого атома. Нижний индекс (ниже) представляет номер каждого атома, в то время как верхний индекс (выше) представляет заряд на данном атоме. Коэффициент перед химической формулой представляет столько единиц молекулы. Каждый из различных типов химической формулы читается немного по-разному.
Типы химической формулы
Эмпирическая формула
Эмпирическая химическая формула представляет относительное число атомов каждого элемента в соединении. Некоторые соединения, такие как вода, имеют одинаковую эмпирическую и молекулярную формулу, потому что они малы и имеют одинаковое соотношение атомов в молекулах и число атомов в молекуле. Эмпирическая и молекулярная формула для воды выглядит следующим образом:
Эмпирическая формула определяется весом каждого атома в молекуле. Поэтому для немного большей молекулы, такой как перекись водорода, эмпирическая формула показывает только соотношение атомов. В этом случае:
Тем не менее, эта эмпирическая химическая формула показывает только базовую основу молекулы. В действительности две молекулы HO: собираются вместе, образуя молекулу перекиси водорода.
Молекулярная формула
Молекулярная формула показывает фактическое количество атомов в каждой молекуле. Таким образом, для перекиси водорода молекулярная формула, таким образом:
H2O2
Как видите, это несколько сбивает с толку фактическую структуру перекиси водорода. В то время как эмпирическая химическая формула дает понять, что молекула имеет два атома кислорода, связанных вместе в середине, молекулярная формула не проясняет это вообще. Тем не менее, молекулярная формула часто используется для описания молекул просто потому, что это удобно, и большинство молекул можно найти после того, как их формула идентифицирована.
Структурная формула
Структурная формула молекулы – это химическая формула с более художественным уклоном. В этих химических формулах показаны фактические связи между молекулами. Это помогает читателю понять, как различные атомы связаны, и, следовательно, как молекула функционирует в пространстве. Есть много различных структурных химических формул для рассмотрения.
Самый простой, метод электронных точек, использует двоеточия и точки, чтобы показать связи между атомами. Каждое двоеточие представляет собой пару электронов, распределенных между атомами по обе стороны от толстой кишки. Эта формула более точно отражает фактическое расположение атомов в молекуле. В случае воды формула электронной точки будет выглядеть следующим образом:
Н: О: Н
Другая химическая формула, формула линии связи, также показывает связи между атомами. Вместо того, чтобы показывать каждый общий электрон, используется линия для обозначения электронной пары, общей для атомов. Вода в формуле линии связи выглядит следующим образом:
Ученые придумали гораздо более продвинутую формулу и представления молекул, включая трехмерные модели типа «шарик-палка», модели заполнения пространства и даже модели, которые учитывают электронную плотность моделируемых атомов. Эти передовые модели учитывают не только присутствующие атомы и их количество, но и углы, размеры и расстояния между атомами в молекуле. Модель воды в виде шарика и стержня ниже даже показывает полярность молекулы, поскольку большой атом кислорода имеет тенденцию притягивать большинство электронов.
Молекулярная масса из химической формулы
Одним из важных навыков, полученных из химической формулы, является расчет молекулярной массы. Молекулярная масса молекулы является суммой всех различных атомов внутри. Каждое вещество имеет определенную молекулярную массу, определяемую его конкретной структурой.
Чтобы определить молекулярную массу вещества, рассмотрим химическую формулу. Формула легко отображает каждый присутствующий атом. Обязательно умножьте на количество атомов каждой молекулы. Индексы на каждом атоме будут указывать, сколько их. Некоторые большие молекулы с несколькими похожими группами покажут группам что-то вроде примера ниже:
C (OH) 4
В этом случае существует четыре группы (ОН), а не 4 атома водорода. Убедитесь, что вы учитываете это при расчете молекулярной массы. Молекулярная масса может использоваться для идентификации веществ, правильного взвешивания веществ для экспериментов и выполнения ряда расчетов, связанных с энергией, участвующей в химических реакциях. Ученые часто используют химическую формулу в качестве хранилища большей части этой информации, без необходимости объяснять основную химию в каждой статье.