дисплазия кишечника 2 степени что это такое лечение
Дисплазия
Дисплазия (от греч. dys — нарушение + plaseo — образую) — неправильное развитие тканей, органов или частей тела.
Она рассматривается как маркер повышенного риска развития онкологического процесса. Выделяют степени дисплазии: слабая, умеренная, тяжелая.
Слабую дисплазию трудно отличить от воспалительного (регенераторного) процесса в эпителии. При затихании воспаления исчезает эта степень дисплазии эпителия. Чтобы убедиться в этом, рекомендуется произвести повторную биопсию после противовоспалительной терапии.
К предраковым изменениям относят лишь дисплазию умеренную и выраженную. Некоторые исследования показали, что умеренная дисплазия является обратимым процессом, но может прогрессировать в тяжелую и наличие ее должно настораживать и обязывать к динамическому наблюдению. Тяжелая, как и средняя, может длительное время оставаться в стабильном состоянии, но лишь иногда подвергается обратному развитию (регрессу), но нередко все же переходит в злокачественный процесс. Чаще всего тяжелая дисплазия выявляется по периферии опухолей, что рассматривается как свидетельство возникновения онкологии на фоне этой тяжелей дисплазии. Умеренная и тяжелая часто сосуществуют и не могут быть четко разделены. Но умеренная, в большинстве случаев возникает в связи с воспалением и регенерацией и значительно чаще, чем тяжелая подвергается регрессии, следовательно надо по возможности диагностировать одну степень от другой, так как от этого зависит прогноз заболевания и судьба пациента.
Маркером онкологии является не дисплазия вообще, а именно тяжелая. Иногда тяжелая дисплазия столь резко выражена, что очень трудно или невозможно по биопсии исключить злокачественность. В таких случаях рекомендуют в гистологическом заключении высказывать предположение о возможной карциноме. Оно обязывает к тщательному наблюдению за больным с повторной биопсией для уточнения диагноза.
Нарушения пищеварения и всасывания в кишечнике в процессе развития белково-энергетической недостаточности у пациентов с дисплазией соединительной ткан
Белково-энергетическая недостаточность широко распространена у пациентов с патологией органов пищеварения, в основе развития которой лежат нарушения кишечного пищеварения и всасывания. В обзоре отражены механизмы белково-энергетической недостаточности у п
Пристальное внимание к избыточной массе тела у пациентов нередко отвлекает врача от такой не менее важной проблемы, как состояние пониженного питания. При оценке прогноза течения заболевания не всегда учитывается наличие дефицита массы тела, питательной недостаточности, степень метаболических нарушений. Существенная роль в развитии белково-энергетической недостаточности принадлежит процессам нарушенного пищеварения и всасывания в кишечнике.
У пациентов с дисплазией соединительной ткани (ДСТ) признаки белково-энергетической недостаточности регистрируются чаще, чем в среднем по популяции [1]. Являясь фоновым заболеванием, ДСТ определяет многообразие морфофункциональных нарушений различных систем органов.
Процесс пищеварения складывается из последовательно сменяемых этапов работы «пищеварительно-транспортного конвейера» [2]:
Нарушения полостного пищеварения (мальдигестия) и всасывания (мальабсорбция) развиваются при различных патологических процессах в желудке, двенадцатиперстной кишке (ДПК), поджелудочной железе, печени, желчевыводящих путях (ЖВП), тонком кишечнике, как органической, так и функциональной природы, и могут захватывать звенья пищеварительной системы как в отдельности, так и комбинированно, тотально, приводя, в конечном итоге, к развитию белково-энергетической недостаточности (рис. 1).
Нарушения полостного пищеварения в кишечнике сопровождают любые моторные нарушения органов пищеварения (как гипер-, так и гипомоторные), встречаются как при недостаточности желудочной секреции, так и при избыточном «закислении» кишечника, недостаточной стимуляции нейропептидной системы и при ее повышенной реактивности. Вторичные воспалительные процессы усугубляют кишечное пищеварение и всасывание. При этом чем выраженнее нарушения пищеварения в кишечнике, тем отчетливее страдает моторная и пищеварительная функция желудка, печени, билиарного аппарата, поджелудочной железы — формируется «порочный круг».
За расстройством полостного пищеварения следуют нарушения пристеночного гидролиза, снижение всасывания нутриентов, витаминов, микроэлеменов, прогрессирует белково-энергетическая недостаточность.
Структурно-функциональные основы мальдигестии у пациентов с ДСТ
Дезорганизация соединительной ткани серозной оболочки, продольного и кругового мышечных слоев, подслизистой, слизистой оболочки полых органов, образующих единый соединительнотканный остов, обусловливает анатомическую вариабельность органов на фоне ДСТ. Аномальные триммеры коллагена чрезвычайно чувствительны к механическим нагрузкам. Изменения размеров, длины органов пищеварения, как правило, рано и в значительной степени отражаются на изменении их функции, снижении сократительной способности с развитием разнообразных гастроэнтерологических синдромов.
Пищеварительная система у пациентов с ДСТ имеет свои анатомические особенности [4]:
Функциональные расстройства органов пищеварения у пациентов с ДСТ характеризуются манифестностью, разнообразием и персистенцией клинической симптоматики, высокой частотой гипомоторных нарушений и рефлюксов [5–11]. В основе моторно-тонических расстройств и клинических проявлений у лиц с ДСТ лежит комплекс диспластикозависимых анатомических изменений пищеварительной системы (анатомическая вариабельность органов, недостаточность сфинктеров). Наличие гастроэнтерологических жалоб и фенотипических признаков ДСТ (астенический тип конституции, наличие торакодиафрагмального синдрома и др.) должно послужить поводом для проведения углубленного исследования органов пищеварения с целью уточнения причины выявленных расстройств.
Кровоснабжение органов пищеварения у пациентов с ДСТ, имеющих дефицит массы тела, отличается более низким объемным кровотоком в системе спланхнитического кровообращения, что в свою очередь усугубляет всасывание и усвоение нутриентов, витаминов и микроэлементов [12].
Терапевтические аспекты
Консервативная терапия включает:
Всем пациентам рекомендуется диета с частым дробным питанием, при наличии спланхноптоза — ношение лечебного бандажа.
Для устранения гипомоторно-гипокинетических расстройств показаны прокинетики (домперидон, итоприд) в стандартных дозах, длительность терапии — до 1 месяца, курсами 2–3 раза в год и/или неселективный агонист опиоидных рецепторов (тримебутин). При наличии запоров показан энтерокинетик прукалоприд.
При наличии аномалий желчного пузыря, гипомоторной дискинезии желчевыводящих путей целесообразно применение препаратов урсодезоксихолевой кислоты. Помимо холеретического действия препараты нормализуют биохимические свойства желчи, конкурентно снижая всасывание гидрофобных (токсичных) желчных кислот в кишечнике, повышают фракционный оборот при энтерогепатической циркуляции, увеличивают концентрацию желчных кислот в желчи, угнетая рост протеолитической кишечной флоры, усиливают желудочную и панкреатическую секрецию, активность липазы, уменьшая проявления относительной панкреатической недостаточности. Образование нетоксичных смешанных мицелл снижает повреждающее действие желудочного рефлюктата на клеточные мембраны при билиарных дуоденогастральных и гастроэзофагеальных рефлюксах. При дискинезии желчевыводящих путей по гипокинетическому типу (и отсутствии диареи) средняя суточная доза — 10 мг/кг в 2 приема в течение от 2 недель до 2 мес. При необходимости курс лечения рекомендуется повторить. При билиарном рефлюкс-гастрите и рефлюкс-эзофагите — по 250 мг/сут перед сном. Лечение от 10–14 дней до нескольких месяцев, курсами.
Наличие синдрома избыточного бактериального роста в кишечнике является обоснованием для назначения антибактериальных препаратов (рифаксимин 200 мг 3–4 раза в сутки 7 дней). Угнетение роста протеолитической флоры сопровождается снижением процессов гниения, подавлением избыточной продукции бактериальных метаболитов, уменьшением выраженности вторичной панкреатической недостаточности. После антибактериальных препаратов назначаются про- и пребиотики. У пациентов с синдромом запора целесообразно назначение лактулозы. При наличии диареи — Saccharomyces boulardii, РиоФлора Баланс, Хилак форте в стандартных дозах. Про- и пребиотики обладают трофическим (стимулирует ферментативную активность кишечных дисахаридаз) и иммуномодулирующим действием. Критериями эффективности терапии являются: улучшение общего состояния, купирование метеоризма, нормализация стула и микробиологических показателей.
Дефицит массы тела, диарея, диспепсические расстройства являются показанием для назначения поликомпонентных ферментных препаратов. Для коррекции диспепсических проявлений, как правило, достаточно использование невысоких доз (до 10 тыс. ЕД липазы) с каждым приемом пищи продолжительностью 2 недели, курсами. Показаниями для назначения препарата Мезим форте у пациентов с ДСТ являются: недостаточность внешнесекреторной функции поджелудочной железы, хронические воспалительно-дистрофические заболевания желудка, кишечника, печени и желчного пузыря. Следует подчеркнуть, что преимуществом препарата Мезим форте перед другими ферментными лекарственными средствами является наличие нескольких лекарственных форм, содержащих соответственно 3 500 ЕД липазы, 10 0000 ЕД липазы и 20 000 ЕД липазы, что позволяет подбирать дозу препарата индивидуально, в зависимости от тяжести расстройства пищеварения. Возможность титрования и подбора минимально необходимой дозы препарата с учетом клинической ситуации позволяет предотвратить развитие функциональной хронической недостаточности поджелудочной железы при использовании высокодозных ферментных препаратов (10 000 ЕД липазы, 25 000 ЕД липазы).
При сохранении энергонутритивного дисбаланса (дисбаланса между потребностями, уровнем поступления и усвоения нутриентов) решить проблему адекватного потребления нутриентов при обычном рационе у ряда пациентов указанными мерами не удается. Наличие синдрома мальабсорбции обосновывает применение препаратов для дополнительного энтерального питания. Предпочтительным является использование полуэлементных смесей (Нутридринк), состоящих из беловых гидролизатов-олигопептидов, ди- и моносахаридов, триглицеридов с длинными и средними углеводородными цепочками, микроэлементов, витаминов.
В 2001 г. Американским обществом клинического питания был представлен метаанализ 90 исследований, 50 из которых были рандомизированными клиническими (РКИ), по использованию дополнительного энтерального питания у пациентов с белково-энергетической недостаточностью различного генеза [13]. В пяти исследованиях (6%, 2 РКИ) отмечено снижение смертности, в 38 исследованиях (42%, 22 РКИ) — улучшение функциональных возможностей, в 64 исследованиях (71%, 35 РКИ) — улучшение антропометрических и биохимических показателей.
Применение ряда фармакологических препаратов (гормона роста и/или анаболических стероидов) нецелесообразно в свете недавнего сообщения о повышенной смертности у тяжелобольных пациентов, получавших гормон роста [14–15].
Таким образом, диспластикозависимые структурно-функциональные особенности пищеварительной системы и висцеральной гемодинамики могут рассматриваться в качестве одной из причин прогрессирования белково-энергетической недостаточности у пациентов с ДСТ. Разнообразие гастроэнтерологических синдромов, многокомпонентность патогенетических механизмов нарушений пищеварения у пациентов с ДСТ требуют особого, взвешенного подхода к курации данной категории пациентов.
Литература
Е. А. Лялюкова, кандидат медицинских наук
ГБОУ ВПО ОмГМА МЗ РФ, Омск
Abstract. Protein-calorie deficiency is typical for patients with alimentary organ pathology. The cause of its development is disturbances of intestinal digestion and absorption. Mechanisms of protein-calorie deficiency of patients with conjunctive tissue dysplasia and approaches to therapy are reviewed in the article.
Новообразования толстого кишечника
Опухоли толстого кишечника бывают доброкачественными и злокачественными. Тубулярная аденома толстой кишки и карциноид аппендикса (червеобразного отростка) относятся к доброкачественным новообразованиям. Аденокарцинома толстой кишки представляет собой злокачественное новообразование, которое развивается из клеток железистого эпителия. Это одна из гистологических разновидностей рака толстой кишки.
В Юсуповской больнице определяют наличие новообразований толстого кишечника с помощью современных методов диагностики. Гистологи верифицируют тип опухоли, исследуя под микроскопом образцы тканей, полученных во время биопсии. При наличии тубулярной аденомы толстой кишки проводят описание микропрепарата.
В зависимости от локализации и гистологического типа опухоли, состояния пациента и наличия сопутствующих заболеваний онкологи вырабатывают индивидуальный план лечения пациента. Тяжёлые случаи карциномы толстой кишки обсуждаются на заседании экспертного совета. В его работе принимают участие кандидаты и доктора медицинских наук, врачи высшей категории. Ведущие онкологи Москвы принимают коллегиальное решение о тактике ведения пациента.
Аденокарцинома может развиться из тубулярно-ворсинчатой аденомы толстой кишки с дисплазией. Последовательность «аденома – рак» подтверждена многочисленными исследованиями учёных. Риск развития злокачественных новообразований прямой и ободочной кишки у лиц с аденоматозными полипами в 3–5 раз выше, чем в общей популяции. В связи с высоким риском злокачественной трансформации тубулярной аденомы толстой кишки с дисплазией онкологи Юсуповской больницы проводят их раннюю диагностику и принимают превентивные меры по снижению заболеваемости аденокарциномой толстой кишки.
Гистологические типы аденом толстого кишечника
Выделяют 3 гистологических типа аденом толстой кишки:
Критерием разделения служит соотношение ворсинчатых и тубулярных структур. Тубулярная аденома толстой кишки – что это такое? Микроскопически тубулярная аденома представлена пролиферирующим аденоматозным эпителием. Опухоль состоит, из ветвящихся и значительно извитых железистых трубочек, более длинных, чем в обычной слизистой кишечника. В тубулярной аденоме присутствует не более 25 % ворсинчатой ткани. Тубулярная аденома толстой кишки имеет покрытое слизистой оболочкой основание. Оно представлено соединительной тканью, гладкомышечными клетками и сосудами. тубулярные аденомы имеют ножку и гладкую дольчатую поверхность. Реже они располагаются на широком основании. Совсем редко встречаются стелящиеся тубулярные аденомы, которые слегка выступают над поверхностью слизистой оболочки.
В тубулярно-ворсинчатых аденомах увеличивается количество ворсинок, которые могут определяться как на поверхности полипа, так и внутри крупных желез. Железы удлиняются, приобретают неправильную форму, плотно прилегают друг к другу. Нарастает степень дисплазии эпителия. В тубулярно-ворсинчатой аденоме процентное содержание ворсинчатой ткани варьирует от 25 до 75 %. Опухоль состоит из выраженных долек, имеет небольшие участки с ворсинками или очень мелкими дольками.
Ворсинчатая аденома состоит из тонких пальцевидных выростов соединительной ткани собственной пластинки слизистой оболочки, которые покрыты эпителием. В ворсинчатых аденомах можно встретить небольшое количество желез и 75% ворсинчатого компонента. Макроскопически ворсинчатые аденомы имеют широкое основание и «мохнатую» поверхность. Существует особый гистологический тип аденомы толстого кишечника – зубчатая аденома. Опухоль близка по строению к гиперпластическому полипу, но обладает возможностью малигнизации.
Аденоматозный эпителий относится к разряду неопластического. По этой причине каждая аденома имеет признаки дисплазии разной степени выраженности. Гистологи различают 3 степени дисплазии тубулярной аденомы толстой кишки:
Тубулярная аденома толстой кишки с дисплазией low grade – это низко дифференцированная опухоль. Она может трансформироваться в аденокарциному.
Классификация
Гистологи выделяют следующие виды злокачественных новообразований толстого кишечника:
Железистый рак принято может быть представлен следующими видами карцином толстой кишки: тубулярными, муцинозными, перстневидноклеточными, плоскоклеточными. Тубулярные аденокарциномы, состоят из трубчатых структур. Опухоли этого вида встречаются более чем у 50% пациентов с железистым раком. Они имеют смазанные контуры и небольшие размеры.
Муцинозная аденокарцинома состоит из слизистых компонентов и эпителиальных структур, не имеет очерченных границ. Метастазирует происходит лимфогенным путем. Высокий риск рецидивирования обусловлен нечувствительностью к радиотерапии.
Перстневидноклеточные аденокарциномы характеризуются высокой агрессивностью клинического течения. Большинство пациентов с опухолями данного вида, которые впервые обращаются за врачебной помощью в Юсуповскую больницу, уже имеет метастазы в лимфоузлах и печени. Онкологическое заболевание чаще всего отмечается у молодых пациентов.
Плоскоклеточные аденокарциномы формируются в области заднепроходного канала. Опухоль состоит из плоских эпителиальных клеток. Для клинического течения плоскоклеточных аденокарцином характерен высокий уровень злокачественности. Они часто рецидивируют, прорастают в ткани влагалища мочеточников, мочевого пузыря, и предстательной железы. Порог пятилетней выживаемости при плоскоклеточных аденокарциномах не превышает 30%.
Причины образования
Развитию тубулярной аденомы толстой кишки способствуют нутритивные факторы: высокое содержание жира и низкое – пищевых волокон. Изменения в рационе питания оказывают влияние на вероятность развития аденомы и аденокарциномы. К нарушению пролиферации эпителиальных клеток могут приводить рафинированные жиры. Нутритивные компоненты, которые содержатся во фруктах, овощах и других продуктах, могут регулировать канцерогенез толстой кишки, влиять на прогрессирование аденомы в карциному.
Увеличение размера полипа, количества ворсинок и выраженная дисплазия повышают риск малигнизации аденомы толстой кишки. Согласно статистическим данным, в аденокарциному преобразуется 4,8 % тубулярных, 22,5 % тубулярно ворсинчатых и 40,7% ворсинчатых аденом. Риск трансформации доброкачественных новообразований в злокачественные опухоли возрастает со степенью дисплазии. 5,7 % аденом со слабой степенью дисплазии, 18 % с умеренной степенью дисплазии и 34,5 % с дисплазией тяжелой степени преобразуются в аденокарциному толстой кишки.
Ворсинчатые, тубулярно-ворсинчатые аденомы и аденомы больше 1 см увеличивают риск последующего развития аденокарциномы толстой кишки. Этот риск выше у пациентов с множественными полипами.
Симптомы и диагностика
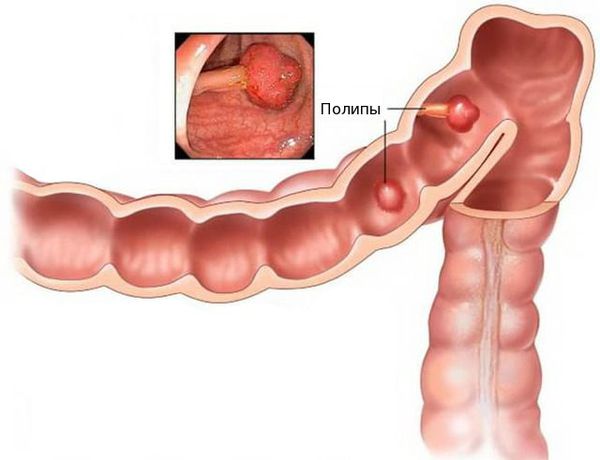
Большинство аденом толстого кишечника клинически не проявляют себя. Их обнаруживают случайно при скрининговых исследованиях или осмотрах по поводу жалоб, которые не связаны с ними. Иногда аденомы вызывают значительные кровотечения или приводят к хронической анемии вследствие длительной скрытой потери крови. Крупные аденомы прямой кишки могут сопровождаться тенезмами, выделением слизи. Продукция слизи в большом объеме вызывает нарушения электролитного баланса. Дистальные аденомы прямой кишки могут выпадать через заднепроходное отверстие.
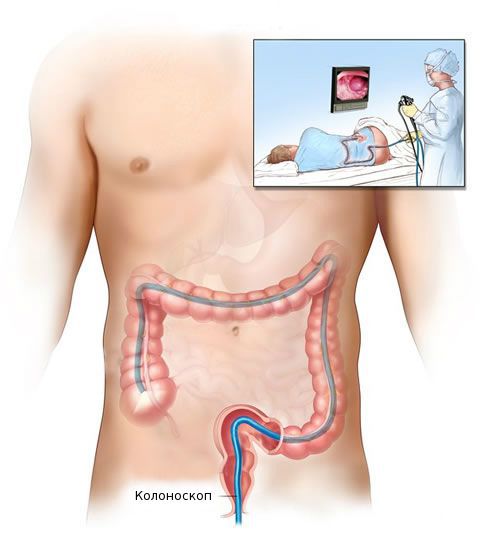
Врачи Юсуповской больницы выявляют аденомы толстой кишки с помощью ректороманоскопии и колоноскопии. Аденома толстого кишечника чаще имеет вид полипа, расположенного на широком основании или связанного со стенкой кишки ножкой. Её длина ножки зависит от темпа роста локализации полипа. Быстро растущие аденомы имеют широкое основание. Медленно растущие расположены на ножке, которая образуется в результате перистальтики и вытяжения полипа перистальтической волной.
Некоторые аденомы толстой кишки имеют углублённый или плоский вид. Они не возвышаются над поверхностью слизистой оболочки. Визуально определить их можно по изменению цвета, структуры слизистой, отсутствию капиллярной сети. В Юсуповской больнице применяют простой и эффективный метод их идентификации – хромоскопию с индигокармином.
Тактика ведения пациентов
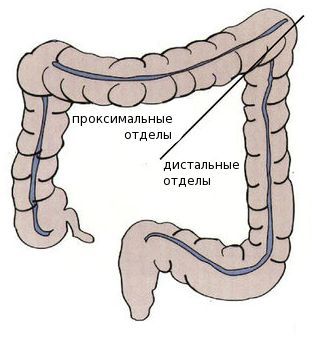
Когда при проведении ректороманоскопии проктологи Юсуповской больницы обнаруживают небольшой полип, размер которого не превышает 1см, выполняют биопсию. Если морфологически верифицируется аденома, проводят колоноскопию для выявления возможных синхронных поражений в проксимальных отделах ободочной кишки. При этом дистальную аденому, выявленную ранее, удаляют. Колоноскопию выполняют даже в том случае, когда при ректороманоскопии выявляют тубулярную аденому толстой кишки небольших размеров.
Если при ректороманоскопии врачи обнаруживают полип размером 1см и более, выполнять биопсию нет необходимости. Новообразование удаляют во время колоноскопии, которую проводят на предмет выявления синхронных опухолевых поражений в верхних отделах толстой кишки. При выявлении неопухолевого полипа (гиперпластического, воспалительного), в последующем наблюдении за ним нет необходимости.
После тотальной колоноскопии и удаления всех полипов последующую колоноскопию проводят через 3 года. При неполном удалении полипа, удалении больших аденом на широком основании, множественных полипов последующие колоноскопии проводят в более ранние сроки. Если при проведении контрольной колоноскопии не обнаруживают новых аденом, интервал наблюдения увеличивают до пяти лет.
При наличии больших полипов на широком основании, при эндоскопическом удалении которых высок риск осложнений, выполняют хирургическое вмешательство с лапаротомного доступа. После полного эндоскопического удаления аденоматозных полипов с тяжелой дисплазией) нет необходимости в дополнительном обследовании или лечении пациентов. Последующую колоноскопию выполняют в течение трёх лет. Если не обнаруживают новых аденом, интервал наблюдения увеличивают до 5 лет.
После эндоскопического удаления аденоматозного полипа с признаками злокачественной опухоли дальнейшую тактику определяют на основании прогностических критериев. Если эндоскопист убеждён, что полип был полностью удалён, при морфологическом исследовании выявлена высокодифференцированная или умеренно дифференцированная аденокарцинома, не было инвазии в кровеносные и лимфатические сосуды, не обнаружено злокачественных клеток в краях резекции, эндоскопическая полипэктомия считается радикальной. Когда отсутствует уверенность в полном удалении аденомы, при морфологическом исследовании выявлена низкодифференцированная аденокарцинома, присутствует инвазия в лимфатические или кровеносные сосуды, обнаружены злокачественные клетки в краях резекции, пациенту проводят оперативное хирургическое вмешательство в связи с высоким риском резидуальной аденокарциномы и метастазов в регионарные лимфоузлы.
При наличии признаков кишечного дискомфорта, причиной которого может быть тубулярная или тубулярно ворсинчатая аденома толстой кишки, высокодифференцированная или низкодифференцированная аденокарцинома, карциноид червеобразного отростка, обращайтесь к онкологам клиники. Вас запишут на приём к врачу Юсуповской больницы. Вы получите консультацию ведущих проктологов, онкологов в удобное для вас время. Своевременное излечение от аденомы толстой кишки предотвращает развитие аденокарциномы.
Что такое аденокарцинома кишки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Мешечкина В. Г., онколога со стажем в 8 лет.
Определение болезни. Причины заболевания
Аденокарцинома толстой кишки — это самая распространённая форма рака прямой кишки, опухоль развивается в толстой кишке и может метастазировать, как и большинство злокачественных новообразований.
Распространённость аденокарциномы толстой кишки
Факторы риска
Основной фактор риска аденокарциномы толстой кишки — возраст старше 65 лет. Риск развития аденокарциномы толстой кишки также возрастает при наличии некоторых наследственных синдромов:
Благоприятным фоном для злокачественного перерождения клеток являются единичные или множественные полипы толстой кишки. Высокий риск перерождения в раковую опухоль имеют аденоматозные полипы. Отказ от их удаления может привести к развитию аденокарциномы.
Хронические воспалительные заболевания толстой кишки, такие как неспецифический язвенный колит и болезнь Крона, также повышают риск развития аденокарциномы.
К дополнительным факторам риска относят:
Симптомы аденокарциномы кишки
Клинические проявления аденокарциномы толстой кишки зависят от расположения опухоли, её типа, темпа роста и наличия сопутствующей патологии. Ранние формы рака являются случайной находкой, так как могут никак себя не проявлять. Их выявляют при эндоскопическом исследовании кишечника по поводу других заболеваний (например, колита, дивертикулита, холецистита, гастрита и др.) или при полостных или гинекологических операциях — аппендэктомии, миомэктомии и кесаревом сечении.
Наиболее частые симптомы аденокарциномы толстой кишки:
Опухоли левого фланка (сигмовидной и прямой кишки, селезёночного угла, нисходящего отдела) чаще манифестируют с запоров, примеси прозрачной или розоватой слизи и тёмной крови в кале, болезненных позывов, отдающих в промежность.
Поиск причины анемии невыясненной этиологии часто приводит к обнаружению рака правой половины толстой кишки.
Патогенез аденокарциномы кишки
Аденокарцинома — это злокачественная опухоль, возникающая из железистых клеток и способная образовывать метастазы (вторичные очаги опухолевого роста). Чаще всего заболевание развивается на фоне длительно существующих полипов, или разрастаний слизистой.
При хроническом повреждении полипов плотными каловыми массами и воспалении развивается дисплазия эпителия (нарушение деления и дифференцировки клеток), переходящая в рак. У кого-то этот процесс может занять десятки лет, у других развивается за два-три года.
Среди пациентов с раком проксимальных отделов толстой кишки преобладают женщины — вероятно, это связано с наличием гормональных рецепторов эстрогенов в этих отделах. Дистальный рак толстой кишки более характерен для мужчин.
Классификация и стадии развития аденокарциномы кишки
Виды аденокарциномы толстой кишки в зависимости от локализации:
Согласно последней классификации ВОЗ, гистологически выделяют две степени злокачественности аденокарциномы толстой кишки, опираясь на долю железистых структур в составе опухоли: высокую и низкую.
Стадирование новообразований толстой кишки по системе TNM-8 (2017 г.) представлено схемой:
Исходя из этих данных, опухоли присваивают определенную стадию, и далее она уже не меняется. Дальнейшее распространение процесса обозначается как прогрессирование.
Осложнения аденокарциномы кишки
Также среди частых причин осложнений выделяют перфорацию и кровотечение из повреждённой опухоли. Это может явиться первым симптомом заболевания. Часто таких пациентов экстренно оперируют в условиях многопрофильного стационара, а не специализированного учреждения, и только при обследовании органов брюшной полости становится понятна причина перфорации.
Диагностика аденокарциномы кишки
Сбор анамнеза
Помимо описанных выше жалоб, с которыми первично обращаются пациенты, важны данные анамнеза. На первичном осмотре терапевту или онкологу следует отметить наличие наследственных синдромов, ассоциированных с раком толстой кишки, и хронических неспецифических воспалительных процессов толстой кишки, например неспецифического язвенного колита или болезни Крона.
Физикальное обследование
При физикальном обследовании, помимо общего осмотра и пальпации брюшной полости, обязательно проведение ректального пальцевого исследования, выявляющего изменения в области прямой кишки. Это один из самых простых диагностических приёмов, не требующий дополнительной подготовки и оборудования.
Лабораторная диагностика
Лабораторная диагностика включает:
Это анализы необходимы для исключения возможной сопутствующей патологии.
Биопсия
После общеклинического обследования проводят уточняющее исследование (биопсию) для определения гистологической структуры опухоли. Чаще всего биопсия выполняется во время колоноскопии — процедуры, при которой врач с помощи эндоскопа осматривает внутреннюю поверхность толстой кишки.
Ирригоскопия и КТ-колонография
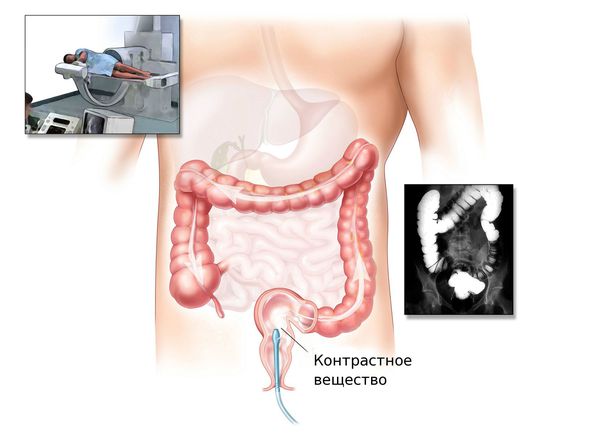
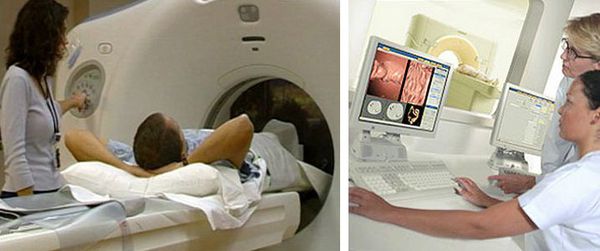
При невозможности проведения колоноскопии врач может назначить ирригоскопию или КТ-колонографию.
Ирригоскопия — это рентгенологический метод обследования толстого кишечника с помощью контрастного вещества, вводимого через прямую кишку.
КТ-колонография — разновидность компьютерной томографии, проводимая при помощи компьютерного томографа.
Компьютерная томография (КТ)
КТ органов грудной клетки и брюшной полости с контрастом — стандарт обследования при раке ободочной кишки. Компьютерную томографию проводят для исключения метастазов в лёгких, лимфоузлах средостения, брюшной полости, канцероматоза (переноса раковых клеток из первичного очага), асцита (скопления жидкости в брюшной полости) и вторичного поражения печени.
Магнитно-резонансная томография (МРТ)
МРТ органов брюшной полости с внутривенным контрастированием применяют для планирования операции на печени при её вторичном поражении.
Для точной оценки размеров опухоли перед операцией и правильного стадирования по TNM проводится МРТ малого таза c применением контраста.
Дополнительно, при наличии болевого синдрома или изменений по КТ, проводится остеосцинтиграфия (ОСГ) — исследование состояния костей скелета.
При подозрении на вторичное поражение головного мозга (исходя из жалоб, осмотра и анамнеза) назначается МРТ головного мозга с внутривенным контрастированием.
Позитронно-эмиссионная томография, совмещённая с компьютерной томографией (ПЭТ/КТ)
ПЭТ-КТ не применяется как рутинный метод при первичной диагностике. Обследование проводят при подозрении на вторичные изменения по данным КТ или МРТ для получения дополнительных данных.
Лечение аденокарциномы кишки
Выбор метода лечения аденокарциномы толстой кишки обусловлен стадией онкологического процесса и наличием или отсутствием соматической патологии.
0-I стадия
На ранних стадиях рака ободочной кишки проводятся органосохраняющие операции, например эндоскопическую резекцию слизистой с удалением в подслизистом слое. При поражении краёв резекции, сосудистой, лимфатической или периневральной инвазии (проникновении раковых клеток в периневрий — слои соединительной ткани, образующие оболочку вокруг пучков нервных волокон), как факторах неблагоприятного прогноза, рекомендуется проведение расширенной операции — повторной резекции краёв.
II–III стадия
При резектабельном (c возможностью удаления) локализованном и местнораспространённом раке ободочной кишки II–III стадий на первом этапе предпочтительно оперативное лечение. Объём хирургического вмешательства определяется индивидуально.
Химиотерапия проводится при поражении лимфатических узлов, прорастании опухолью серозной оболочки и соседних органов, наличии факторов риска.
При распространённом раке ободочной кишки с резектабельными или потенциально резектабельными синхронными метастазами в печени или лёгких выполняют R0-резекцию (в пределах здоровых тканей).
Радиочастотная абляция и стереотаксическая лучевая терапия применяются как дополнительные методы к резекции печени и как самостоятельные методы лечения. Действие радиочастотной абляции основано на нагревании с помощью радиоволн поражённых тканей до высоких температур (90–100 °С).
Стереотаксическая лучевая терапия — это один из видов радиохирургии, который состоит в применении высокоточного излучения, воздействующего на опухоли.
При резектабельных очагах рекомендуется их одномоментное хирургическое удаление.
На послеоперационном этапе при резектабельных метастатических очагах показано проведение адъювантной (следующей за операцией) химиотерапии. Также возможно проведение дооперационной химиотерапии до шести циклов, удаление метастазов и первичной опухоли с дальнейшим продолжением химиотерапии до достижения шестимесячной суммарной продолжительности лечения.
IV стадия
Основная цель лечения на IV стадии заболевания — перевод при помощи химиотерапии нерезектабельных метастазов в резектабельные. Хороший эффект даёт добавление к основному лечению таргетной терапии ( целенаправленно воздействующей на специфические мишени в опухолевых клетках) и иммунотерапии.
При проведении нерадикальной резекции возможно продолжение терапии предоперационной комбинацией химиопрепаратов и моноклональных антител (препаратов, избирательно воздействующих на определённую молекулу, от которой зависит развитие болезни ) до достижения суммарной шестимесячной продолжительности лечения.
При генерализованном раке ободочной кишки с нерезектабельными метастазами применяют комбинацию химиопрепаратов. Возможно добавление таргетных препаратов. Цель лечения — максимально долго контролировать развитие заболевания при сохранении качества жизни.
При проведении химиотерапии каждые 1,5-2 месяца оценивают резектабельность опухоли (по данным КТ, МРТ). При преобладании метастатического поражения печени проводят:
Прогноз. Профилактика
Меры профилактики:
_575.gif)