кальцинаты серпа мозга что это
Кальцинаты серпа мозга что это
Физиологические внутричерепные кальцификаты на снимках в переднезадней и боковой проекциях:
Эпифиз
Кальцифицированный эпифиз обнаруживают у 5% детей в возрасте младше 10 лет и почти у двух третей взрослых. Они имеют аморфный или кольцевидный вид и существенно варьируют по размеру, но обычно меньше 1 см. Кальцификат эпифиза, превышающий I см в диаметре, указывает на новообразование либо пинеалому или даже чаще на тератому.
Уздечка эпифиза
расположена на несколько миллиметров кпереди эпифиза и почти у трети пациентов кальцифицирована. Кальцифицированная уздечка принимает характерную форму буквы «С», открытой кпереди. Смещение уздечки внутричерепными объемными образованиями происходит тем же путем, что и смещение эпифиза.
Кальцификаты каменисто-клиновидной и межклиновидной связок
Кальцификаты каменисто-клиновидной и межклиновидной (диафрагма седла) связок часто возникают у пожилых. Первая лежит между кончиком спинки седла и вершиной каменистой части височной кости, тогда как последняя может формировать межклиновидный (седла) мостик.
Хориоидные сплетения
Хориоидные сплетения могут кальцифицироваться во всех желудочках, чаще всего это происходит в преддверной части боковых желудочков (соединение тела бокового желудочка с задним и височным рогами), проецирующейся в боковой проекции приблизительно на 2-3 см позади и немного ниже эпифиза. В переднезадней проекции кальцификаты сплетения проецируются приблизительно на 3 см от средней линии и обычно симметрично, хотя некоторое неравенство в размерах между разными сторонами иногда присутствует. Величина кальцификации может значительно варьировать и не имеет клинического значения. Распространенные кальцификаты сплетений могут обнаруживаться при нейрофиброматозе.
Кальцификация твердой мозговой оболочки
Кальцификация твердой мозговой оболочки, черепа и/или намета возникает приблизительно в 10% случаев, и каждый вариант имеет свои характерные признаки. Кальцификация твердой мозговой оболочки вокруг сагиттального синуса имеет V-образную форму у вершины на снимке в переднезадней проекции. Кальцификаты в этой области иногда могут быть вызваны кальцифицированными пахионовыми (паутинными) грануляциями (дивертикулоподобными выпячиваниями паутинного пространства, прободающими твердую мозговую оболочку и проецирующимися на просвет основных синусов и прилежащих венозных озер).
Кальцификаты серпа
В норме располагаются кпереди и четко видны как линейные полосы или пластинки на одном или обоих листках серпа. На снимках в переднезадней проекции кальцификаты по свободному краю намета имеют форму перевернутой буквы «V». Величина кальцификации твердой мозговой оболочки, серпа и намета обычно не имеет клинического значения, особенно когда кальцификация более или менее диффузная.
Кальцификаты серпа и твердой мозговой оболочки обнаруживают у двух третей пациентов с синдромом базально-клеточного невуса (Горлина—Гольтца), а распространенные кальцификаты твердой мозговой оболочки упоминают при эластической псевдоксантоме.
Из книги «Опухоли мозга. КТ- и МРТ-диагностика». Посмотреть/заказать
Обызвествление серпа мозга может приводить к формированию локальных крупных кальцинатов, костной плотности, которые со временем могут приобретать структуру губчатой кости (головка стрелки на рис.1041,1042). Обызвествление так же может быть вытянутой стелящейся вдоль ТМО формы (стрелки на рис.1044) с характеристиками МР-сигнала подобными диплоическому веществу (рис.1044-1045). Кроме того, может встречаться дисэмбриогенетический жир вдоль серпа мозга (стрелки на рис.1043), о чём свидетельствуют отрицательная плотность на КТ. Петрификация ТМО появляться с возрастом и может возникать спустя годы после операции (рис.1046), отражая кровяное пропитывание и инкрустацию дуры.
Кальцификаты гипофиза
Кальцификаты гипофиза редко распознают на снимках черепа в отличие от гистологического исследования. На снимках черепа они могут иметь вид камней.
Артериосклеротические кальцификаты
Артериосклеротические кальцификаты внутренней сонной артерии часто видны в месте ее прохождения через пещеристые синусы. Такие кальцификаты могут варьировать по размеру от мелких хлопьев, достигая полной визуализации каротидного сифона. На снимках в боковой проекции такие кальцификаты накладываются на изображение турецкого седла, тогда как кольцевидные кальцификаты могут быть видны на одной из сторон седла на снимках в переднезадней проекции.
Кальцификаты базальных ганглиев
Кальцификаты базальных ганглиев обнаружива ют при многих заболеваниях, но чаще всего их обнаруживают случайно у здоровых взрослых людей. Они не имеют клинического значения. Кальцификаты различают по размеру от точечных до слившихся затемнений с характерным расположением: на снимках в переднезадней проекции кальцификаты располагаются симметрично парасагиттально, тогда как на снимках в боковой проекции они могут принимать незначительно изогнутую форму и примерно располагаться параллельно чешуйчатому шву. Склероз по ходу чешуйчатого шва на снимках в боковой проекции иногда имеет вид полосовидного затемнения не следует путать с кальцификатами базальных ганглиев.
Кальцификаты в зубчатых ядрах мозжечка встречаются реже, чем в базальных ганглиях, но обнаруживаются при тех же состояниях. На боковом снимке черепа такие кальцификаты часто маскируются воздушными ячейками сосцевидного отростка, но лучше всего они видны в окципитальной (Тауне) проекции в виде симметричных полулунных затемнений.
Кальцинаты серпа мозга что это
а) Терминология:
1. Сокращения:
• Болезнь Фара (БФ)
2. Синонимы:
• Семейная идиопатическая кальцификация базальных ганглиев
• Двусторонняя стриопаллидодентатная кальцификация
• Идиопатический семейный цереброваскулярный феррокальциноз
3. Определение:
• Редкое дегенеративное заболевание нервной системы:
о Протяженная двусторонняя кальцификация (Са++) базальных ганглиев (БГ)
о Может привести к развитию прогрессирующей дистонии, паркинсонизма, нейропсихиатрических нарушений
1. Общие характеристики болезни Фара:
• Лучший диагностический критерий:
о Двусторонняя симметричная кальцификация БГ, таламусов, зубчатых ядер и белого вещества больших полушарий при КТ
• Локализация:
о Бледный шар = наиболее частая локализация отложения Са++
— Латеральные отделы бледного шара > медиальные отделы бледного шара
о Также вовлекаются в процесс скорлупа, хвостатые ядра, таламусы, мозжечок (в частности, зубчатые ядра), внутренние капсулы, белое вещество больших полушарий
• Морфология:
о Вариабельная степень выраженности
о Контуры локальной компактной кальцификации часто соответствуют границам БГ
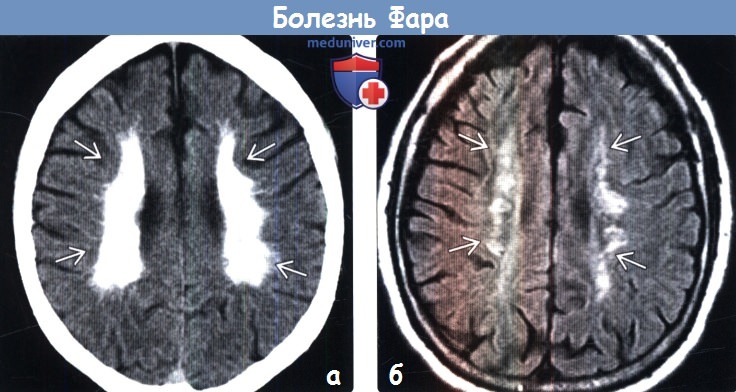
(б) МРТ, FLAIR, аксиальный срез: у этого же пациента в зонах кальцификации определяется повышение интенсивности сигнала. В случаях с выраженной степенью заболевания гиперинтенсивные поражения могут распространяться на весь полуовальный центр.
2. КТ признаки болезни Фара:
• Бесконтрастная КТ:
о Двусторонняя симметричная кальцификация типичной локализации
• КТ с контрастированием:
о Накопление контраста отсутствует
3. МРТ признаки болезни Фара:
• Т1-ВИ:
о Вариабельная интенсивность сигнала в зависимости от:
— Стадии заболевания, количества осажденного кальция
— Индивидуальных различий в метаболизме кальция
о Зона кальцификации обычно имеет гиперинтенсивный на Т1-ВИ сигнал
• Т2-ВИ:
о Локальная компактная кальцификация может проявляться ги-по-/гиперинтенсивным сигналом
о Гиперинтенсивные участки в белом веществе:
— Не соответствуют участкам отложения кальция
— Могут отражать метаболический или воспалительный процесс в мозговой ткани, который впоследствии переходит в кальцификацию
— Весь полуовальный центр может иметь гиперинтенсивный сигнал у пациентов с деменцией
— Очаги во внутренних капсулах могут коррелировать с контрлатеральным гемипарезом
• FLAIR:
о Те же изменения, что и на Т2-ВИ
• SWI:
о Выраженное снижение интенсивности сигнала
о SWI может быть более чувствительным методом, чем КТ
4. Радионуклидная диагностика болезни Фара:
• ПЭТ:
о Может наблюдаться двустороннее ↓ захвата ФДГ в БГ:
— Также наблюдается в коре лобных и височно-теменных областей, а также в области гиппокампа
о При болезни Фара (БФ) функциональные аномалии могут предшествовать морфологическим изменениям
• ОФЭКТ с Тс-99-этилцистеинат димером (ЭЦД):
о ↓ перфузии в очагах кальцификации:
— Особенно в условиях деменции
— Не связано с объемом отложений кальция
о При проведении исследования во время проявления симптомов может наблюдаться ↑ перфузии:
— Особенно в височных долях (на фоне слуховых галлюцинаций)
5. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о Бесконтрастная КТ
• Совет по протоколу исследования:
о МРТ с SWI может оказаться более информативным методом
в) Дифференциальная диагностика болезни Фара:
1. Норма:
• Симметричная кальцификация БГ у людей среднего, пожилого возраста
• Бледные шары
• Обычно имеет точечный характер, но может быть довольно массивной
• Обнаруживается при КТ и не имеет клинического значения
• Чрезвычайно частая находка у пациентов старшей возрастной группы
• Если кальцификация наблюдается и в других областях предполагайте патологическое состояние
3. Патологическая кальцификация БГ:
• Эндокринологические нарушения:
о Гиперпаратиреоз, гипопаратиреоз, псевдогипопаратиреоз, псевдопсевдогипопаратиреоз, состояние после тиреоидэктомии
о Аналогичная БФ локализация отложения кальция
о Гипопаратиреоз: ↑ ионизированного кальция в интерстиции в сочетании со ↓ уровня циркулирующего кальция
о Кальцификация при первичном гипопаратиреозе имеет более диффузный характер, чем при других ее причинах
о Кальцификация при гипопаратиреозе после тиреоидэктомии имеет более локальный характер
• Нейропсихиатрические нарушения (например, при системной красной волчанке, болезни моторных нейронов)
• Постинфекционные нарушения (например, при ТБ, токсоплазмозе, цистицеркозе)
• Интоксикация (например, отравление угарным газом, свинцом)
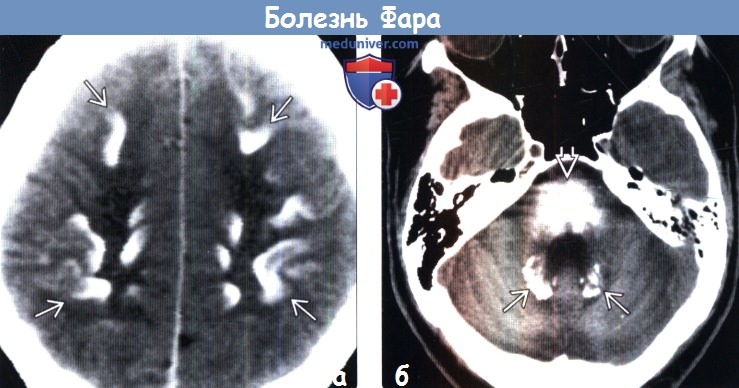
(б) Бесконтрастная КТ, аксиальный срез: при болезни Фара (которая, как и в данном случае, имеет семейный характер) отмечается как типичная кальцификация зубчатых ядер, так и нетипичная и чрезвычайно гиперденсная кальцификация среднего мозга.
1. Общие характеристики болезни Фара:
• Этиология:
о Кальцификация структур ЦНС при БФ может отражать:
— «Метастатическое» отложение кальция вследствие местного нарушения гематоэнцефалического барьера
— Нарушение метаболизма кальция в нейронах
о Нарушение переноса железа и свободные радикалы → поражение ткани → кальцификация
• Генетика:
о У большинства семей с БФ аутосомно-доминантный тип наследования:
— Иногда аутосомно-рецессивный характер
о БФ часто имеет семейный, но гетерогенный характер:
— У членов одной семьи могут обнаруживаться вариабельная экспрессивность и сниженная пенетрантность, однако у большинства пациентов заболевание имеет симптоматический характер
— «Генетическое ожидание» = в многопоколенной семье возраст дебюта заболевания ↓ с каждой его передачей
— У большинства членов некоторых родов заболевание имеет бессимптомное течение
о Первый локус идентифицирован: BGC1 на 14q:
— Регион BGC1 содержит более 100 известных генов, маркерные экспрессирующие последовательности и предсказанные гены
— На данный момент стало известно, что это не главный локус
2. Стадирование и классификация:
• Болезнь Фара = идиопатические кальцификация с когнитивными и нейроповеденческими проявлениями:
о Диагноз исключения; для его постановки необходимо выявление нормальных уровней кальция, фосфора и паратиреоидного гормона
• Синдром Фара = те же проявления, что и при БФ, но развивается вторично по отношению к другим состоянием (например, гипопаратиреозу)
3. Микроскопия:
• Характерные признаки: диффузная кальцификация нейрофибриллярных сплетений (также известная как кальцификация типа Фара) о Нейрофибриллярные сплетения, содержащие тау-белок и фосфорилированный тау-белок
• Преобладающим элементом является кальций:
о Также присутствуют и другие элементы (Zn, Р, Fe, Mg, Al, К)
• Са++ во внеклеточном, внесосудистом пространствах, часто вокруг капилляров:
о Кальцификация медиальных стенок и адвентиции
о Отложение кальция в участках демиелинизации, отложение липидов
о Са++ связывается с белками или полисахаридами
д) Клиническая картина:
1. Проявления болезни Фара:
• Наиболее частые признаки/симптомы:
о Нейропсихиатрические нарушение
о Когнитивные нарушения (подкорковая деменция)
о Экстрапирамидные двигательные нарушения
• Клинический профиль:
о Метаболизм Са++/Р, уровень паратгормона в норме
о Обычно бессимптомное течение в первые два десятилетия жизни, несмотря на наличие множественных кальцификатов в головном мозге
о Неврологические проявления имеют вариабельный характер, однако двигательные нарушения встречаются наиболее часто:
— Чаще наблюдается паркинсонизм, обычно имеет постоянный и прогрессирующий характер
— Также имеются сообщения о преходящем паркинсонизме у детей
— Пароксизмальный дистонический хореоатетоз
2. Демография:
• Возраст:
о Дебют симптомов обычно происходит в возрасте 30-60 лет
о Также описана инфантильная форма
о Два варианта клинической манифестации:
— Ранний взрослый возраст (шизофреноподобный психоз)
— 6-е десятилетие жизни (экстрапирамидный синдром, подкорковая деменция)
• Пол:
о Половая предрасположенность отсутствует
• Эпидемиология:
о Встречается редко
3. Течение и прогноз:
• Характеризуется очень медленным прогрессированием
• Ухудшение когнитивного статуса и потеря моторных навыков:
о Дегенеративное заболевание, а не нарушение развития
• БФ с дебютом во взрослом возрасте: отложение кальция начинается в третьем десятилетии жизни с неврологическим ухудшением два десятилетия спустя
• Симметричный спастический паралич, а иногда и атетоз после своего появления переходят в децеребрационное состояние
• Обычно развиваются нейропсихиатрические нарушения
• Предлагаемый «обрыв» в таламо-кортико-стриатарной цепи ведет к «синдрому разъединения», названному «когнитивная дисметрия», который проявляется симптомами шизофрении
е) Диагностическая памятка:
1. Обратите внимание:
• Предполагайте БФ у пациентов с паркинсонизмом, деменцией и симптомами поражения мозжечка
• Кальцификация БГ у пациента
Редактор: Искандер Милевски. Дата публикации: 28.4.2019
Физиологические интеркраниальные обызвествления
Физиологическая интеркраниальная кальцификация очень распространена, и данная тема хорошо изучена в последние десятилетия. И нтеркраниальная кальцификация связана со старением головного мозга.
Наиболее частая локализация физиологического обызвествления:
Встречается у 2/3 взрослого населения. Количество кальцификации увеличивается с возрастом. Кальцинаты более 1 см в диаметре и обызвествление у детей моложе 9 лет наводят на мысли об новообразовании.
Хабенулярная комиссура играет центральную роль в регуляции лимбической системы. У 15% взрослого населения в виде криволинейного паттерна кальцификации, расположенный кпереди от шишковидного тела, размером не больше нескольких миллиметров.
Очень частая находка у пациентов в возрасте до 40 лет. Обызвествления сосудистых сплетений III и IV желудочков наблюдаются редко.
Кальцификаты в базальных ганглиях — это обычно случайная находка, которая встречается с частотой
1% (диапазон 0.3-1.5%) и чаще встречается у пациентов в пожилом возрасте. Кальцификаты в базальных ганглиях до 30 лет связывают с заболевания метаболического генеза.
Кальцификация выше перечисленных анатомических элементов встречается в 10% случаев у пожилого населения.
Кальцификация каменисто-клиновидной связки связана с возрастной дегенерацией и визуализируется в виде ламинарного или узелкового паттерна.
Кальцификация верхнего сагиттального синуса связана с возрастной дегенерацией и визуализируется в виде ламинарного или узелкового паттерна.
Болезнь Фара
Болезнь Фара — идиопатическая симметричная кальцификация церебральных структур: подкорковых ганглиев, коры полушарий, мозжечка. Может протекать бессимптомно, клинически проявляется экстрапирамидными расстройствами (гиперкинезами, паркинсонизмом), мозжечковыми нарушениями, интеллектуальным снижением. Диагностируется по данным церебральной КТ при исключении вторичного характера кальцинированных очагов по результатам биохимических, ультразвуковых, ПЦР исследований. Лечение симптоматическое с применением средств, улучшающих тканевый обмен, цитопротекторов, препаратов леводопы, антиконвульсантов.
МКБ-10
Общие сведения
Болезнь Фара включает случаи первичного идиопатического отложения кальция в мозговых структурах, вторичные формы церебрального кальциноза в рамках данной патологии не рассматриваются. Первые подробные описания заболевания сделаны в 1930 году немецким невропатологом К.Т. Фаром. Болезнь Фара является редкой нозологией, распространённость составляет менее 1 случая на 1 млн. населения. Гендерные различия в заболеваемости выражаются соотношением мужчин и женщин 2:1. Патология проявляется в любом возрастном периоде, чаще в 30-60 лет. Прижизненно выявляется лишь в 1-2% случаев, что объясняется наличием бессимптомных вариантов течения, диагностикой заболевания под видом иных нейродегенеративных процессов (болезни Паркинсона, сенильной хореи).
Причины болезни Фара
Патогенез
Формирующие болезнь патогенетические механизмы окончательно не определены. Предполагаются генетически детерминированные сдвиги церебрального метаболизма, становящиеся причиной отложения в мозговых тканях избытков кальция. Выраженная кальцификация подкорковых образований становится причиной дезорганизации лобно-субкортикальной системы, регулирующей произвольные движения и обеспечивающей когнитивные функции (память, мышление, внимание).
Морфологически кальцификаты обнаруживаются симметрично в различных структурах: коре мозга, белом веществе, подкорковых ганглиях, внутренней капсуле, мозжечке, стенках мелких артерий, реже вен. Характерно наличие периваскулярных мелких кальциевых конгломератов. Наиболее массивная кальцификация выявляется в подкорковых отделах. Микроскопически кальцификаты отличаются типичной структурой, представленной нитями толщиной 140-400 мкм. Они зачастую содержат минеральные комплексы с включениями железа, меди, алюминия, фосфора, свинца, цинка, кобальта.
Классификация
В практической неврологии болезнь Фара подразделяется на две клинические формы, отличающиеся возрастом манифестации, типом преобладающей симптоматики:
Симптомы болезни Фара
В типичных случаях болезнь дебютирует появлением утомляемости, неуклюжести движений, шаткости ходьбы, изменений речи, непроизвольных двигательных актов или ночных мышечных спазмов. Основу клинических проявлений составляют экстрапирамидные нарушения. В молодом возрасте это различные гиперкинезы: атетоз — непроизвольные червеобразные движения в пальцах кистей, хореоатетоз — сочетание атетоза с быстрыми насильственными движениями в конечностях, торсионная дистония — тонические мышечные спазмы, придающие телу неестественные позы. У взрослых наблюдается вторичный паркинсонизм: амимия лица, брадикинезия, замедленные скованные движения, шаркающая походка, постуральный тремор.
Симптоматика паркинсонизма зачастую сочетается с мозжечковой атаксией (дискоординация, несоразмерность движений, нистагм), пирамидной недостаточностью (слабость в конечностях, повышенные сухожильные рефлексы, патологические стопные знаки). Возможна дизартрия, дисфагия, недержание мочи. Эпилептические пароксизмы более характерны для ювенильной формы заболевания, могут отмечаться у взрослых.
Сопровождающие болезнь Фара когнитивные нарушения характеризуются снижением памяти на текущие и прошлые события, замедленным мышлением, неустойчивым вниманием, угасанием способности к аналитической и синтетической интеллектуальной деятельности. Прогрессирование расстройств когнитивной сферы у детей приводит к олигофрении, во взрослом возрасте — к развитию корково-подкорковой деменции с элементами агнозии, апраксии, алексии. Однако часть больных ювенильной формой остаются интеллектуально сохранными.
Диагностика
Основным диагностическим методом, позволяющим неврологу достоверно установить наличие очагов кальциноза в мозговых тканях, является КТ головного мозга. Интенсивность очагов на томограммах отражает уровень концентрации кальция. МРТ головного мозга значительно хуже визуализирует кальцификаты, но позволяет оценить сопутствующие дегенеративные процессы. С целью подтверждения идиопатического характера патологии проводится целый ряд дополнительных обследований:
Диагноз болезнь Фара правомочен после исключения вторичного характера церебральной кальцификации, наблюдающейся при эндокринных (гипопаратиреоз, псевдогипопаратиреоз, гипотиреоз), сосудистых (атеросклероз, амилоидоз сосудов), инфекционных (краснуха, цистицеркоз, токсоплазмоз, цитомегалия) заболеваниях. Дифференциальная диагностика проводится также с болезнью Галлервордена-Шпатца, туберозным склерозом.
Лечение болезни Фара
Поскольку патогенез заболевания остаётся неясным, терапия имеет преимущественно симптоматический характер. С целью улучшения обменных процессов применяются стимуляторы тканевого метаболизма (ацетилкарнитин, глютаминовая кислота, комплекс L-цитруллин+малат, никотинамид), цитопротекторы (рибофлавин, янтарная кислота, мельдоний). При симптомах паркинсонизма предпочтительно назначение фармпрепаратов леводопы, при гиперкинезах — холинолитиков, бензодиазепинов. Наличие эпилептических приступов служит показанием к лечению современными антиконвульсантами (леветирацетамом). В комплексной терапии применяется лечебная физкультура, водолечение, когнитивные тренинги.
Прогноз и профилактика
Клинически проявленная болезнь Фара рассматривается как хроническое нейродегенеративное заболевание. Прогноз выздоровления неблагоприятный, однако, при должном уровне поддерживающей симптоматической терапии состояние пациентов длительное время остаётся удовлетворительным. Субклинический вариант не сказывается на здоровье и когнитивных способностях больного, может быть случайной находкой при проведении компьютерной томографии. Специфические меры, позволяющие предупредить развитие болезни, не разработаны.
Кальцинаты серпа мозга что это
Процессы, протекающие в головном мозге, вероятно, относятся к самым сложным для изучения. Патологические изменения, происходящие в его структурах, являются наиболее труднодиагностируемыми, несмотря на наличие современного оборудования и обширных познаний врачей в данной области. Болезнь Фара относится к редким и малоизученным заболеваниям, которые затрагивают преимущественно базальные ганглии, мозжечок и полушария головного мозга.
Болезнь Фара – идиопатическая неатеросклеротическая симметричная интрацеребральная кальцификация коры полушарий, базальных ганглиев и зубчатых ядер мозжечка, связанная с отложением солей кальция и железа в стенках мелких артерий и артериол, а также в вещество головного мозга. Морфологически кальцификаты обнаруживаются симметрично в различных структурах: коре мозга, белом веществе, подкорковых ганглиях, внутренней капсуле, мозжечке, стенках мелких артерий, реже вен [1].
Характерно наличие периваскулярных мелких кальциевых конгломератов. Наиболее массивная кальцификация выявляется в подкорковых отделах. Микроскопически кальцификаты отличаются типичной структурой, представленной нитями толщиной 140–400 мкм [2].
Впервые синдром (или болезнь) Фара был диагностирован в конце 1930 г. немецким врачом-неврологом Карлом Теодором Фаром. Это редкое дегенеративное заболевание, его распространенность составляет, как было сказано ранее, порядка 1 случая на 1 млн населения. При этом мужчины болеют приблизительно в 2 раза чаще.
Разнообразие симптоматики данного заболевания объясняет сложность постановки диагноза. Клинически болезнь может протекать как совершенно бессимптомно, так и с яркими экстрапирамидными нарушениями в виде мышечной ригидности, тремора, судорог, схожими с таковыми при болезни Паркинсона [3, 4]. Для больных характерны гиперкинезы, головокружения, шаркающая походка. Именно схожесть с другими распространенными заболеваниями затрудняет своевременное выявление данной патологии [5, 6].
На современном этапе развития системы здравоохранения с увеличением доступности компьютерной томографии в рутинной неврологической практике диагностика феррокальциноза постепенно увеличивается, однако, по литературным данным, в большинстве случаев обнаружение кальцинатов является находкой, а не диагностической необходимостью.
Этиология болезни Фара установлена не до конца. Возможными причинами считают гормональные нарушения при патологии щитовидной и паращитовидной желез, что ведет к дисбалансу ионов кальция и фосфора: чаще всего – первичный или вторичный гиперпаратиреоз, реже – псевдогиперпаратиреоз при продукции паратгормона опухолевой тканью (при бронхогенном раке, раке молочной железы); при локализации опухоли в костной ткани (множественная миелома, метастазы в кости). Еще одним из механизмов возникновения предполагают дыхательный алкалоз, компенсируемый фосфатной буферной системой: внутриклеточная концентрация фосфатов увеличивается, в то время как в плазме крови возникают относительная гиперкальциемия и абсолютная гипофосфатемия [7, 8].
Указывается, что гипоксия мозга при гипертонической болезни и атеросклерозе церебральных артерий может приводить к локальному увеличению концентрации ионов кальция в веществе мозга и вызывать петрификацию нейронов базальных ганглиев, но, по мнению авторов, данная гипотеза является исключительно теоретической, а на практике – безосновательной.
Также предполагают возможность генетического характера патологии с локализацией нарушений в четырнадцатой (локус 14q13), второй (локус 2q37) хромосомах, хромосомном участке q21.1-q11.23 восьмой хромосомы. Были установлены варианты, когда болезнь наследовалась аутосомно-доминантным и Х-сцепленным путем [9]. Важно отметить, что имели также место и случаи, в которых семейный характер патологии не прослеживался.
Имеется описание дебюта болезни Фара у пациентки на фоне пневмонии, вызванной SARS-CoV-2 (COVID-19) [10].
Диагностировать болезнь Фара позволяет проведение биохимического анализа крови. Производятся определение электролитов крови: кальция, фосфора, железа, натрия; определение уровня паратгормона; ПЦР-исследования для выявления токсоплазмы, цитомегаловируса и других инфекционных агентов, способных вызывать воспалительные изменения тканей мозга с образованием кальцификатов.
Ключевое значение в диагностике болезни Фара имеют инструментальные методы исследования – УЗИ щитовидной и паращитовидных желез, компьютерная томография и рентгенография.
Лечение заболевания проводят только симптоматически. При симптомах паркинсонизма назначают предшественники дофамина (леводопу), при гиперкинезах – холинолитики (циклодол), в случае эпилептических состояний – барбитураты (фенобарбитал) и бензодиазепины (феназепам, лоразепам, клоназепам). С целью улучшения обменных процессов применяют стимуляторы тканевого метаболизма (глютаминовую кислоту, никотинамид), цитопротекторы (рибофлавин, янтарную кислоту).
В работе нами был проанализирован случай диагностики болезни Фара по результатам аутопсии. Пациентка женского пола М., 1949 года рождения, поступила в ГБУЗ СГКБ № 1 им. Н.И. Пирогова с жалобами на общую слабость, головокружение, мышечные спазмы, тошноту, рвоту, повышенную температуру. При поступлении состояние средней тяжести. При осмотре кожные покровы бледные, видимые слизистые физиологической окраски, зев гиперемирован. Дыхание везикулярное, ЧДД – 12 в минуту, ЧСС – 79 в минуту, пульс ритмичный, АД – 135/75 мм рт. ст., температура 37,4°C. Пациент в сознании, на контакт идет, внимание рассеянное, лицо симметричное, походка неуверенная, наблюдается тремор верхних конечностей. В отделении проведено обследование в полном объеме.
Результаты анализов на ВИЧ, гепатиты B и C отрицательны. В общем анализе крови отклонений от нормы не выявлено. В ходе биохимического анализа крови обнаружены следующие изменения: гипергликемия (глюкоза – 9,2 ммоль/л), гиперкальциемия (кальций – 3,1 ммоль/л), гипокалиемия (калий – 3,2 ммоль/л).
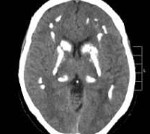
Компьютерная томография головного мозга: геморрагический инсульт в области базальных ядер справа и слева, двусторонняя симметричная кальцификация базальных ганглиев, таламусов, зубчатых ядер и белого вещества больших полушарий.
Макроскопическая картина центральной нервной системы по результатам аутопсии
Кости свода и основания черепа целые. Твердая мозговая оболочка не напряжена, гладкая, сероватая. Мягкая мозговая оболочка отечная, полнокровная. Полушария мозга симметричны. Мозг весом 1410 г. Борозды незначительно углублены. Сосуды основания мозга с единичными атеросклеротическими бляшками на интиме, стенозирующими просвет до 20%. В области базальных ядер головного мозга справа – участок дрябловатой ткани мозга диаметром 1 см с единичными кровоизлияниями диаметром до 1 мм. Выражено полнокровие мелких сосудов. Желудочки мозга незначительно расширены, эпендима гладкая, в просвете прозрачный ликвор. На миндалинах мозжечка следы давления краев большого затылочного отверстия. Во всех других отделах анатомический рисунок строения вещества головного мозга хорошо выражен, с четкой границей и обычным соотношением серого и белого вещества. Ткань мозга на разрезе влажная, блестящая; в области базальных ядер – издает характерный хруст – звон.
Гистологическое исследование головного мозга
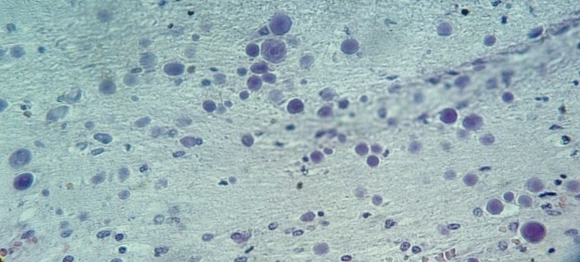
В микропрепарате коры головного мозга – многочисленные зернистые шары (рис. 1).
В микропрепаратах базальных ганглиев – неравномерное кровенаполнение, диапедезные кровоизлияния вокруг сосудов (рис. 2А), умеренный периваскулярный и перицеллюлярный отек (рис. 2А-Б).
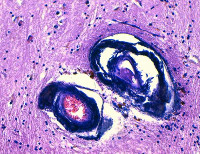
Стенки сосудов деформированные (рис. 3А), со множественными консолидированными (рис. 3А) и пылевидными (рис. 3Б) кальцинатами в виде концентрических преимущественно равномерно распределенных колец между адвентицией, средней оболочкой и пограничной мембраной глии.
Рис. 1. Препарат коры головного мозга пациента женского пола, страдавшего болезнью Фара, умершего от геморрагического инсульта. Многочисленные зернистые шары. Окраска гематоксилин-эозином. Увеличение х200
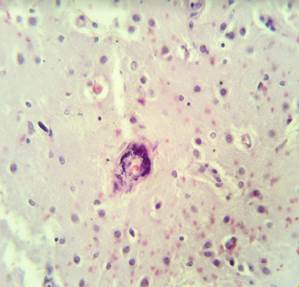
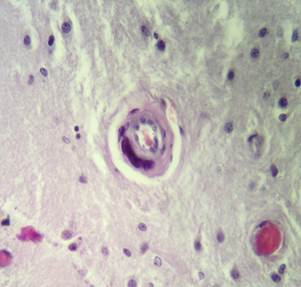
Рис. 2. Препарат базальных ядер пациента женского пола, страдавшего болезнью Фара, умершего от геморрагического инсульта. А – диапедезные кровоизлияния вокруг кальцинированных сосудов с деформированной стенкой, умеренный перицеллюлярный отек. Б – кальцинированный сосуд, умеренный перицеллюлярный и периваскулярный отек. Окраска гематоксилин-эозином. Увеличение х200
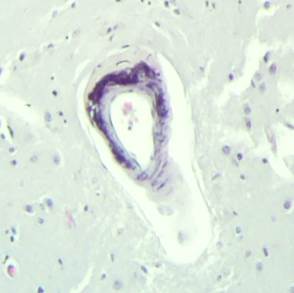
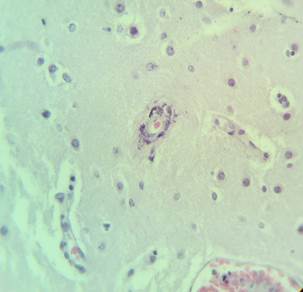
Рис. 3. Препарат базальных ядер пациента женского пола, страдавшего болезнью Фара, умершего от геморрагического инсульта. А – консолидированные кальцинаты в стенке сосуда, выраженный периваскулярный отек. Б – пылевидные кальцинаты в стенке сосуда, умеренный перицеллюлярный и периваскулярный отек. Окраска гематоксилин-эозином. Увеличение х200
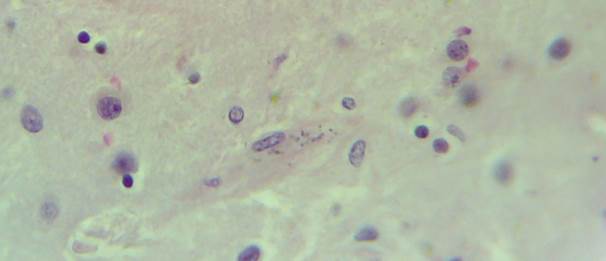
Кальцинаты обнаружены в артериях мелкого и среднего калибра, а также в единичных венах (рис. 4А-Б). В веществе мозга и перинейронально имеются кальцинаты в форме различных по размерам глыбок округлой формы (рис. 4Б – крупные кальцинаты, рис. 5 – пылевидные кальцинаты в веществе мозга). Отдельные нейроны кальцинированы.
Со стороны сердечно-сосудистой системы определена концентрическая гипертрофия миокарда (масса сердца 360 г, толщина стенки левого желудочка 1,7 см, правого – 0,4 см, гистологически – гипертрофия мышечных волокон, диффузное разрастание мелких полос соединительной ткани), атеросклероз аорты и ее ветвей, стенозирующий атеросклероз коронарных артерий (III стадия, 3-я степень, стеноз до 30% правой и левой коронарных артерий).
В правом надпочечнике макроскопически определяется округлое образование диаметром 1,2 см, на разрезе равномерного желтовато-оранжевого цвета, гистологически – светлоклеточная аденома надпочечника.
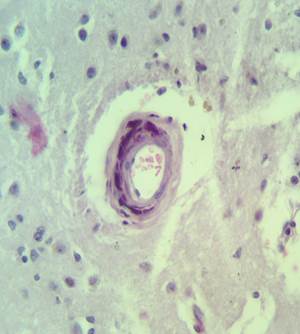
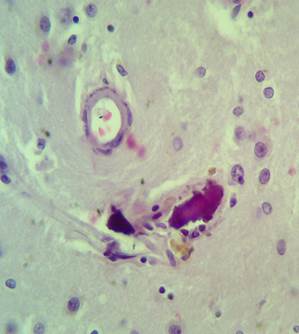
Рис. 4. Препарат базальных ядер пациента женского пола, страдавшего болезнью Фара, умершего от геморрагического инсульта. А – консолидированные и пылевидные кальцинаты в стенке сосуда, выраженный периваскулярный и умеренный перицеллюлярный отек. Б – пылевидные кальцинаты в стенке сосуда, крупный перинейрональный кальцинат, слабый перицеллюлярный и периваскулярный отек. Окраска гематоксилин-эозином. Увеличение х250
Рис. 5. Препарат базальных ядер пациента женского пола, страдавшего болезнью Фара, умершего от геморрагического инсульта. Пылевидные кальцинаты в веществе головного мозга. Окраска – гематоксилин-эозином. Увеличение х400
При анализе данного клинического случая мы склонны считать болезнь Фара и артериальную гипертензию важнейшими сочетанными нозологическими единицами, безусловно повлиявшими на танатогенез. Повышение давления в кальцинированных сосудах мелкого калибра, не обладающих должной эластичностью, приводит к развитию очаговых кровоизлияний.
В связи с разнообразной неспецифической неврологической симптоматикой, а часто и полным отсутствием каких-либо проявлений болезнь Фара остается одним из малоизученных нейродегенеративных заболеваний.
Разработанные и в целом доступные методы диагностики позволяют выявлять феррокальциноз пациентов, однако ограниченность серьезных генетических и лабораторных методов диагностики, низкая приверженность к назначению компьютерной томографии пациентам без клиники острого нарушения мозгового кровообращения объясняют позднюю выявляемость данной патологии; наличие специфической макроскопической и микроскопической картины обусловливает выявление болезни Фара почти исключительно по данным аутопсии.