классификация по bethesda system nilm что значит
Скрининг рака шейки матки
Изменения шейки матки при раке и предопухолевых состояниях часто протекают бессимптомно и обычный осмотр не всегда укажет на патологию. Скрининговые программы позволяют своевременно выявить изменения, определить причину и назначить лечение.
Предрасположенность к раку шейки матки определяется генетическими маркерами, но вклад в развитие патологии составляет не более 1% из всех случаев. Большое влияние оказывают внешние и внутренние факторы. Нарушения гормонального фона и питания ткани, локальное состояние иммунитета — определяют внутреннюю причину, по которой возникают предраковые изменения. Ранняя активная половая жизнь, частая смена половых партнеров и частые роды, применение гормонсодержащих контрацептивных препаратов, наличие ИППП в анамнезе являются внешними факторами риска развития рака шейки матки.
В 85% случаев рак шейки матки ассоциирован с ВПЧ.
ВПЧ и рак шейки матки
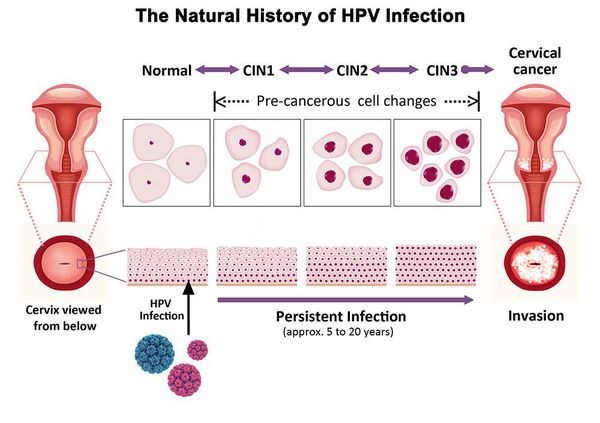
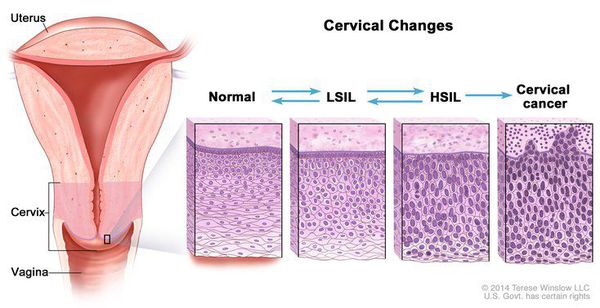
ВПЧ — ДНК-содержащий вирус. Вирус обладает родством к эпителиальным клеткам. После проникновения в клетки, вирус запускает синтез собственного генетического материала. Зараженные эпителиальные клетки начинают активно делится. Но из-за нарушений, клетки эпителия остаются незрелыми. Эпителиальный пласт не формируется должным образом. Возникает дисплазия.
В шейке матки в 90% случаев вирус может элиминироваться из организма благодаря внутренним резервам организма женщины. Но длительное нахождение вируса в клетках в 10% случаев провоцирует цервикальные интраэпителиальные неоплазии (CIN). Выделяют три гистологических класса CIN: легкой (CIN I), умеренной (CIN II) и высокой степени (CIN III), при переходе одной в другую вероятность формирования рака увеличивается. Дисплазии легкой степени (CIN I) в 90% случаев инволюционируют в нормальную ткань или остаются в неизменном виде, 10% прогрессируют в CIN II. CIN II трансформируются в CIN III в 1 случае из 10. При персистенции ВПЧ более 3-х лет на фоне дисплазии высокой степени развивается рак. Такая ситуация наблюдается у половины женщин с диагнозом инвазивный рак.
Существует около 200 видов ВПЧ, но не каждый тип способен вызвать поражения шейки матки. ВПЧ 16 и 18 типов обычно выявляются при цервикальной интраэпителиальной неоплазии CIN III и инвазивном раке, поэтому назван вирусом высокоонкогенного типа. ВПЧ 6 и 11 типа часто ассоциирован с CIN I и CIN II и обладает низким онкогенным потенциалом.
| Наличие дисплазии выявляется при проведении цитологического исследования по Папаниколау (ПАП-мазок). В ходе анализа изучаются особенности строения клеток, их морфология, расположения, после чего выдается заключение о наличии или об отсутствии атипии клеток. Для выполнения анализа материал должен быть получен с трех участков: влагалищной части шейки матки, цервикального канала и зоны трансформации. Зона трансформации — зона перехода многослойного плоского эпителия шейки матки в железистый эпителий цервикального канала. В зоне трансформации обычно начинаются предраковые изменения. |  |
Полученный материал переносится на предметное стекло и окрашивается, после чего врач-цитолог исследует образец под микроскопом. Если мазок, не содержит цилиндрический эпителий, то образец считается неинформативным и исследованию не подлежит.
Процесс забора мазка не стандартизован, поэтому могут быть получены ложноотрицательные результаты. Для того, чтобы избежать ложных ответов, нужно соблюдать правила забора образца. Ответственность лежит на медицинском персонале, результат зависит от квалификации человека.
Ответственность за правильную подготовку к исследованию лежит на пациенте. Перед сдачей мазка на цитологию женщина должна придерживаться простых правил подготовки:
В таком случае образец не будет содержать посторонних элементов, и лаборатория сможет выдать достоверное заключение.
Результат цитологического анализа
Цитологическая интепретация клеточного состава должна быть представлена лечащему врачу в клинически значимых терминах и определениях. Существует несколько цитологических классификаций. Наиболее распространенные это классификация по Папаниколау и Бетдеста.
В соответствии с классификацией Папаниколау мазки делятся на 5 типов:
Классификация Бетесда является международной. Она создана в качестве унифицированного инструмента передачи информации между врачами-цитологами и врачами-клиницистами.
В классификации Бетесда введен термин «плоскоклеточные интраэпителиальные поражения»(SIL), которые могут быть высокой и низкой степени (LSIL и HSIL соответственно). LSIL соответствует слабой дисплазии (CIN I) и папилломавирусной инфекции. HSIL объединяет умеренную (CIN II) и тяжелую дисплазии (CIN III), внутриэпителиальный рак.
Образец, в котором клетки трудно поддаются дифференцировке, и врач не может определить связаны ли изменения с дисплазией или это реактивное состояние, выводятся в класс ASC-US. При постановке такого диагноза пациентка должна находится под динамическим наблюдением.
Если врач-цитолог видит, что в эпителии присутствуют изменения доброкачественные и нет никаких настораживающих морфологических признаков, выводит в заключении NILM. NILM также обозначает норму и реактивные изменения.
Соответствия цитологических заключений: корреляция между классификацией дисплазией/карциномой in situ/, Bethesda system 2001 года и классификацией по Папаниколау.
ПАП-тест. О чем говорят аббревиатуры?
Каждая женщина, которая хоть раз была у гинеколога, знает, что на приеме у нее обязательно возьмут мазки, в том числе на цитологическое исследование. Во многих случаях только после комплексного обследования шейки матки — расширенной кольпоскопии, мазков на флору и цитологию и при необходимости биопсии — специалист сможет установить диагноз и назначить оптимальный метод лечения.
Термином «дисплазия», или «неоплазия», уже не удивишь женщин, даже далеких от медицины. Они понимают, что речь идет о наличии атипичных клеток, которое может быть как при злокачественном, так и доброкачественном процессе.
И все же, когда держишь в руках результат мазка с непонятными аббревиатурами, волнение есть всегда.
Что такое цитологический скрининг и почему его нужно проходить каждой женщине, расскажет онкогинеколог Больницы израильской онкологии LISOD Инна Субботина.
— Инна Витальевна, расскажите, что такое ПАП-тест и как часто его необходимо проходить?
— ПАП-тест, который также называют цитологическим скринингом, помогает своевременно выявить предраковые состояния шейки матки средней и тяжелой степени и пролечить их. Регулярное обследование с началом половой жизни значительно снижает риск заболеть раком шейки матки. В большинстве стран мира ПАП-тест рекомендуют проходить раз в три года с 21-летнего возраста, но украинские врачи считают целесообразным начинать его в Украине раньше, с 18 лет, а завершать в 65 лет, как и в большинстве стран мира. Это обусловлено определенными эпидемиологическими особенностями: ранним началом половой жизни, распространенностью различных форм иммунодефицита, чрезвычайно низким уровнем вакцинации от ВПЧ и большим количеством случаев курения среди женщин.
— Нужно ли готовиться к сдаче ПАП-теста?
— Лучше проходить обследование в первые сухие дни после менструации. Для женщин, которые принимают противозачаточные таблетки, неважно, в какой день цикла проходить тест, а женщины в менопаузе могут проходить его в любой удобный день. За 48 часов до теста нужно исключить половые отношения, не использовать вагинальные свечи, орошения, гели и кремы.
ПАП-тест — это безболезненная процедура. Некоторые женщины могут испытывать дискомфорт и ноющие боли внизу живота во время забора анализа. Это нормально.
Забор клеточного материала проводится специальной щеточкой, которая помещается в контейнер с фиксирующим транспортным раствором или наносится тонким слоем на предметное стекло. Первые, но уверенные шаги делает в Украине котестинг (одновременное цитологическое исследование и определение вируса папилломы человека (ВПЧ) методом полимеразной цепной реакции).
— Какими могут быть результаты этого исследования? Что рекомендуется при каждом из них?
— Для описательного цитологического заключения используется классификация Bethesda, согласно которой проводится интерпретация результатов:
Нередко женщины и особенно — молодые девушки обращаются с непонятным для них результатом цитологического обследования шейки матки и с волнующим вопросом «Что делать дальше?» При получении любого из результатов ПАП-теста есть абсолютно четкие и научно обоснованные методы дообследования и тактики ведения пациенток, которые основываются на международных рекомендациях и данных доказательной медицины.
Если вы получили результат «неудовлетворительная цитология согласно классификации Bethesda», рекомендуется повторить ПАП-тест через 2-4 месяца (независимо от возраста).
Заключение ASCUS (Atipical Squamous Cells of Undetermined Significance, атипичные клетки плоского эпителия неясного значения) — характеризует такие структурные изменения в клетках, которых качественно и количественно недостаточно для постановки диагноза CIN. Это означает, что цитологическая картина не позволяет дифференцировать изменения плоского эпителия между реактивными и диспластическими, то есть предраковыми. У большинства больных с такими результатами в течение наблюдения клеточный состав нормализуется, однако 10-20% прогрессируют в дисплазию. Однако риск развития тяжелой дисплазии CIN ІІІ у женщин с ASCUS и отрицательным результатом на ВПЧ (-) не превышает 1-2%, поэтому такие пациентки наблюдаются без применения инвазивных методик обследования, а тактика наблюдения зависит от возраста и наличия или отсутствия высокоонкогенных типов ВПЧ при исследовании урогенитальных выделений.
Результат скрининга ASC-H (Atypical Squamous Cells Can not Exсlude HSIL, атипичные клетки плоского эпителия, которые не исключают HSIL) — независимо от ВПЧ-статуса рекомендуется расширенная кольпоскопия, а при любых признаках поражения показана биопсия, цервикальный кюретаж. У женщин пери- и менопаузального возраста, если зона перехода плоского и цилиндрического эпителия шейки матки кольпоскопически НЕ визуализируется, а кюретаж не дал достоверной информации, — как диагностическая мера может рассматриваться конизация шейки матки. Такое вмешательство должен выполнять специалист экспертного уровня. Дальнейшая тактика зависит от результатов гистологического исследования.
ПАП-тест с результатом CIN I или LSIL (Low-grade Intraepitelial Lesion, поражение эпителия легкой степени) — цитологические изменения, обусловленные ВПЧ (койлоцитоз) и неспецифические воспалительные изменения. CIN І часто регрессирует самостоятельно, поэтому в этой группе пациенток чаще всего применяется тактика динамического наблюдения. Однако необходимо обязательно выполнить ВПЧ-тест для определения дальнейшей тактики.
Для женщин с результатом CIN I и ВПЧ (-) рекомендуется цитологический контроль через 6 мес., возможен двойной тест «котестинг» через 12 мес. Если через 12-18 мес. по результатам наблюдения получаем NILM — рекомендуется перейти к рутинному скринингу.
Для женщин с CIN І / ВПЧ (+) рекомендована кольпоскопия, и при обнаружении тяжелого поражения эпителия шейки матки — биопсия, а при его отсутствии — повторный цитологический контроль через 6 мес. или двойной тест через 12 мес. У таких пациенток необходимо создать условия для элиминации ВПЧ: рекомендовано прекратить курение, при необходимости — провести лечение хронических инфекций, коррекцию вагинального микробиома — кандидоза, бактериального вагиноза, хронической герпетической инфекции и т. п. Стоит помнить, что у 12-25% ВПЧ (+) женщин с CIN І в течение 4 лет может произойти прогрессия в CIN более тяжелых степеней.
При наличии цитологического заключения CIN IІ и CIN ІІІ или HSIL в 70-80% случаев у пациенток оказывается CIN ІІ / ІІІ в гистологическом материале после биопсии и цервикального кюретажа, а в 1-3% — инвазивный рак. Поэтому независимо от ВПЧ-статуса всегда рекомендуется кольпоскопия, обязательно подготовленным специалистом, биопсия измененных участков — под контролем кольпоскопии, эндоцервикальный кюретаж у небеременных с последующим морфологическим исследованием полученного материала. Рекомендовано также кольпоскопическое обследование влагалища. В случаях с цитологическим результатом CIN ІІ / ІІІ, если при кольпоскопии не обнаружено изменений или выявлено поражение легкой степени, рекомендуется биопсия и эндоцервикальный кюретаж (если он не выполнялся до того) и / или диагностическая коническая биопсия.
Как исключение — девушки моложе 21 года. Риск инвазивного рака у них чрезвычайно низкий, кольпоскопия и цитология должны быть проведены повторно через 3-6 месяцев, при условии, что кольпоскопия адекватная, то есть визуализируется зона трансформации, а эндоцервикальный кюретаж отрицательный.
Перед проведением инвазивных вмешательств всегда рекомендуется проведение тестирования на носительство вируса иммунодефицита человека (ВИЧ), поскольку именно эти женщины в группе повышенного риска по цервикальным неоплазиям.
— Что делать при гистологическом подтверждении легкой или средней и тяжелой дисплазии шейки матки?
— В случае выявления при биопсии поражения низкой степени LSIL (легкой дисплазии, CIN I) и при удовлетворительных результатах кольпоскопии (зону трансформации 1-го типа видно полностью) возможны два подхода: наблюдение — рекомендуется в большинстве случаев или активное лечение, которое может рассматриваться при признаках длительной персистенции CIN І.
Наблюдение — оптимальная тактика ведения, особенно молодых женщин и тех, которые планируют беременность. Заключается она в цитологическом контроле + ВПЧ-тестировании + кольпоскопии каждые 6 мес., пока не будет цитологических и кольпоскопических доказательств регрессии легкой дисплазии. Стоит отметить, что у пациенток с нелеченной CIN І существует 13% риск обнаружения CIN ІІ, CIN ІІІ в течение двух лет наблюдения.
Хирургическое, а именно эксцизионное лечение CIN І может быть предложено пациенткам при длительной персистенции поражения более 18 мес., особенно с положительным ВПЧ-статусом и у женщин старше 30 лет; пациенткам, которые не имеют репродуктивных планов и отказываются проходить регулярный контрольный гинекологический осмотр; женщинам с положительным ВИЧ-статусом.
При гистологическом подтверждении HSIL, то есть CIN ІІ и CIN ІІІ тактика лечения чаще склоняется к хирургическому вмешательству. Однако стоит помнить, что около 40% случаев CIN ІІ могут регрессировать в течение 2 лет, особенно у молодых женщин. Регрессия CIN ІІІ происходит крайне редко.
Рекомендации по лечению при тяжелой дисплазии CIN ІІІ единодушны: обязательное удаление патологически измененного участка шейки матки, то есть эксцизия / конизация у небеременных пациенток. Единственное исключение — HSIL (CIN II) у девушек младше 21 года, при отсутствии положительного ВИЧ-статуса, поскольку у молодых пациенток высокая вероятность регрессии. В этой категории больных желательно также проведение иммуногистохимического исследования индекса пролиферативной активности с использованием моноклональных антител к белку р16 или р16 / Кі67 для уточнения биологического потенциала диспластических изменений эпителия шейки матки. Наблюдение возможно при отсутствии гиперэкспрессии р16 не более 12 мес. При персистенции HSIL (CIN II) и ВПЧ (+) более 12 мес. рекомендовано применение эксцизионных методов лечения. Хирургическое лечение HSIL (CIN II / III) может проводиться подготовленными специалистами экспертного уровня под контролем кольпоскопии.
Поскольку шейка матки покрыта не только плоским, но и цилиндрическим железистым эпителием, который расположен в цервикальном канале, соответственно здесь тоже случаются проблемы онкологического характера.
Цитологическое заключение ПАП-теста — AGC (цервикальное интраэпителиальное поражение железистых клеток) и АIS (аденокарцинома in situ) в каждом случае требует консультации цитолога, онкогинеколога, гинеколога экспертного уровня.
Атипичные железистые клетки в цитологическом мазке могут иметь эндоцервикальное происхождение, то есть из шейки матки, или эндометриальное, то есть из полости матки. Поэтому всем пациенткам этой группы рекомендуется расширенная кольпоскопия и цервикальный кюретаж. Обследование в возрасте старше 35 лет включает обязательный эндометриальный кюретаж или гистероскопию, тем более при наличии сопутствующей экстрагенитальной патологии (ожирение + сахарный диабет + гипертоническая болезнь), патологических маточных кровотечений и обремененного раком семейного анамнеза.
При наличии атипии железистых клеток или AIS в биопсии, но без признаков инвазивного рака, может рассматриваться конизация шейки матки как метод выбора у молодых пациенток с репродуктивными планами на будущее однако женщинам, которые реализовали свою репродуктивную функцию и не планируют в дальнейшем рожать, рекомендована гистерэктомия — удаление матки, особенно с подтвержденной гистологически AIS, с учетом высокой вероятности неполного удаления поражения при конизации (до 26%) или инвазивного рака (1,2%), частых рецидивов заболевания после лечения, мультифокальной природы болезни и малоинформативности цитологических проявлений AIS.
Помните, что при своевременном выявлении рака шейки матки болезнь имеет благоприятный прогноз по лечению и полному выздоровлению, поэтому о собственном здоровье в первую очередь должны позаботиться вы сами!
Пройти обследование у гинеколога, сдать все необходимые анализы, сделать ПАП-тест и при необходимости пройти лечение выявленных предраковых заболеваний можно в Больнице израильской онкологии LISOD. Лучшие онкогинекологи дадут подробную консультацию по результатам анализов и назначат эффективное лечение.
Запишитесь на консультацию:
0-800-500-110 — бесплатно по Украине;
Что такое дисплазия шейки матки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Игнатенко Т. А., гинеколога со стажем в 13 лет.
Определение болезни. Причины заболевания
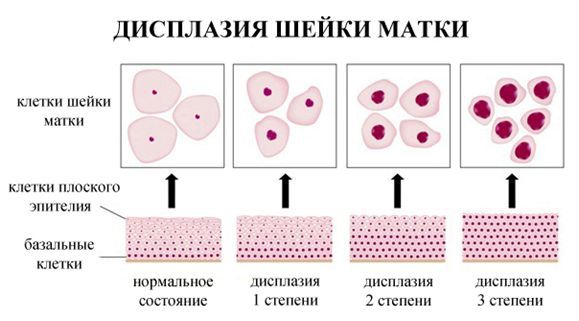
Дисплазия шейки матки, или цервикальная интраэпителиальная неоплазия (ЦИН), или Cervical Intraepithelial neoplasia (CIN) — это патологический процесс, при котором в толще клеток, покрывающих шейку матки, появляются клетки с различной степенью атипии (неправильного строения, размера, формы).
Основной фактор развития дисплазии и рака шейки матки — папилломавирусная инфекция (ПВИ), причем длительное персистирование именно ВПЧ высокого канцерогенного риска. У женщин с риском развития цервикальной неоплазии распространенность онкогенных типов ВПЧ чрезвычайно велика. ВПЧ становится причиной CIN 2-3 и рака шейки матки в 91,8% и 94,5% случаев соответственно. [1]
Риск цервикальной CIN 2 особенно высок у женщин, которые до этого имели опыт пересадки органов, у них выявлена ВИЧ-инфекция или они принимают иммунодепрессанты. [2]
Кроме того, была выявлена связь между пассивным курением среди некурящих и повышенным риском возникновения CIN 1. [3]
Симптомы дисплазии шейки матки
Дисплазия шейки матки, как правило, имеет бессимптомное течение, поэтому пациентки не предъявляют никаких специфических жалоб.
Патогенез дисплазии шейки матки
Критический фактор развития цервикальной интраэпителиальной неоплазии — инфицирование вирусом папилломы человека. Во многих случаях цервикальная интраэпителиальная неоплазия легкой степени отражает временную реакцию организма на папиломавирусную инфекцию и без лечения исчезает в течение полугода-года наблюдения. При цервикальной интраэпителиальной неоплазии умеренной и тяжелой степени высока вероятность встраивания вируса папилломы человека в клеточный геном. Инфицированные клетки начинают продуцировать вирусные белки E6 и Е7, которые продлевают жизнь клетки, сохраняя ее способность к неограниченному делению. Неизбежно формирующиеся на этом фоне мутации клеток ведут к формированию предрака (дисплазии) и рака шейки матки, влагалища и вульвы.
Онкогенные белки ВПЧ (Е6, Е7) взаимодействуют с регуляторными белками клеток шейки матки, приводя к повышению активности онкомаркера p16INK4A, что свидетельствует о неконтролируемом размножении клеток шейки матки. Таким образом, сверхэкспрессия p16INK4A, определяемая в материале шейки матки, который получают при биопсии, является биомаркером интеграции вируса папилломы человека высокого риска в геном и трансформации эпителиальных клеток под действием вируса, что делает эту информацию полезной при оценке прогноза развития предраковых и злокачественных поражений, связанных с инфицированием генитального тракта вирусом папилломы человека. [5]
Классификация и стадии развития дисплазии шейки матки
Для постановки цитологического диагноза (по результатам цитологического исследования соскобов шейки матки и цервикального канала с окрашиванием по Папаниколау (Рар-тест) или жидкостной цитологии) используется классификация Бетесда (The Bethesda System, 2014), основанная на термине SIL (Squamous Intraepithelial Lesion) – плоскоклеточное интраэпителиальное поражение. [10]
Выделяют три вида результатов соскобов с поверхности шейки матки (экзоцервикса):
Классификация Папаниколау
Существуют также гистологические классификации для оценки материала, полученного при биопсии.
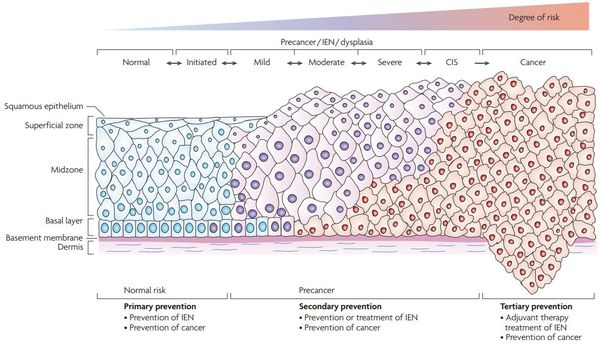
По классификации R. M. Richart (1968) в зависимости от глубины поражения поверхностного клеточного слоя шейки матки выделяют:
В приведенной ниже таблице даны соотношения классификаций предраковых поражений шейки матки. [9]
Осложнения дисплазии шейки матки
Основное и самое опасное осложнение цервикальной интраэпителиальной неоплазии заключается в развитии рака шейки матки, любой случай развития которого — результат упущенных возможностей диагностики и лечения дисплазии шейки матки. [7]
Проводились длительные, систематические исследования риска рака шейки матки у женщин с диагнозом цервикальной интраэпителиальной неоплазии 3 степени (CIN3) по сравнению с женщинами, у которых были нормальные цитологические результаты. Согласно полученным данным, долгосрочный относительный риск развития рака шейки матки зависит от различных гистологических типов CIN3 и выше всего он для аденокарциномы in situ. Даже через 25 и более лет после конизации (хирургического иссечения патологических тканей шейки матки) риск злокачественного перерождения клеток был значительным. [4]
Диагностика дисплазии шейки матки
Для ранней диагностики предраковых поражений шейки матки во многих странах мира существует система цервикального скрининга.
В России данная система включает последовательность действий:
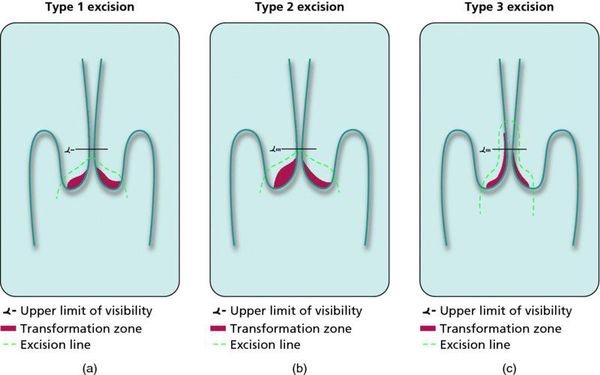
При кольпоскопии должна быть тщательно оценена зона трансформации (переходная зона стыка двух видов покровного эпителия шейки матки).
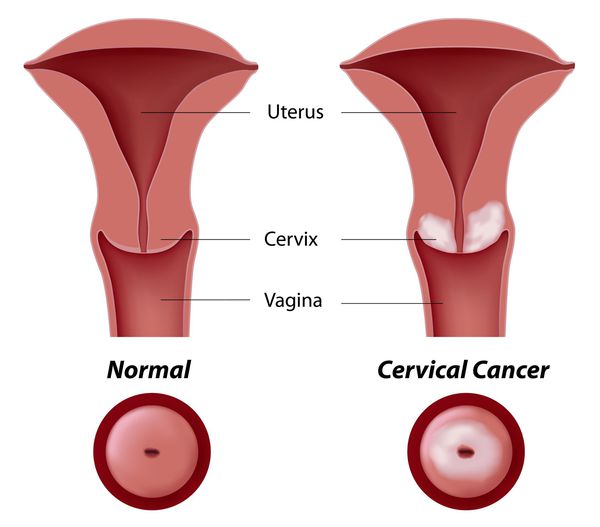
Влагалищная часть шейки матки (экзоцервикс) покрыта многослойным плоским эпителием. В канале шейки матки (цервикальном канале, эндоцервиксе) — цилиндрический эпителий. Место перехода цилиндрического эпителия цервикального канала в многослойный плоский эпителий поверхности шейки матки носит название зоны трансформации. Эта область имеет большое клиническое значение, поскольку именно в ней возникает более 80% случаев дисплазии и рака шейки матки.
Лечение дисплазии шейки матки
Динамическому наблюдению подлежат молодые пациентки (до 35 лет) с LSIL (ВПЧ, ЦИН 1, ЦИН 2, если при биопсии не обнаружен белок р16, являющийся признаком проникновения ВПЧ высокого риска в геном и трансформации опухолевых клеток под действием вируса). Наблюдать возможно пациенток только с 1 и 2 кольпоскопическим типом зоны трансформации.
Контрольные осмотры, цитологическое и ВПЧ-тестирование показаны через 6 и 12 месяцев после первичного обнаружения патологии. При выявлении HSIL (ЦИН 2 c обнаружением белка р16 при биопсии, ЦИН 3) неизбежно хирургическое лечение в виде абляции («прижигания») или эксцизии (удаления) поврежденной ткани. Для абляции используют электро-/радио-, крио- и лазерные воздействия. Эксцизия возможна электро-/радиоволновая или ножевая.
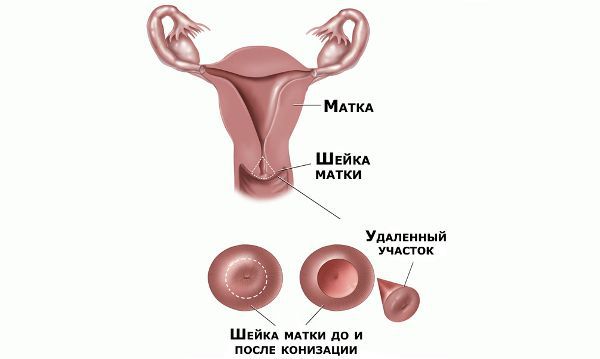
Немаловажно, что при выявлении по кольпоскопии 3 типа зоны трансформации на фоне положительного РАР-теста гинеколог обязан провести выскабливание слизистой канала шейки матки и/или широкую эксцизионную биопсию (конизацию шейки матки) для исключения опухолевого процесса, потенциально располагающегося вне зоны кольпоскопического обзора. Немаловажно наблюдение после операции через 6 и 12 месяцев с выполнением цитологического соскоба и ВПЧ-теста.
Следует отметить, что процедура хирургического иссечения патологических тканей на шейке матки увеличивает риск преждевременных родов. А сама по себе цервикальная интраэпителиальная неоплазия первой степени на течении беременности и родов никак не отражается и зачастую опасности не представляет. [12]
Средний возраст женщин, когда может потребоваться хирургическая коррекция цервикальной внутриэпителиальной неоплазии — около 30 лет. Хирургическое лечение нередко ассоциировано с неблагоприятным течением последующей беременности. Частота и тяжесть неблагоприятных осложнений возрастают с увеличением глубины иссекаемых тканей. [13]
Прогноз. Профилактика
При своевременном выявлении и лечении дисплазии шейки матки прогноз благоприятный. Основным фактором развития и прогрессирования дисплазии шейки матки является длительное инфицирование канцерогенными типами ВПЧ. Для предупреждения заражения ВПЧ существуют профилактические вакцины «Церварикс» (защита от 16, 18 типов ВПЧ), «Гардасил» (профилактика инфицирования 6, 11, 16, 18 типами вируса), в декабре 2014 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов одобрило использование вакцины «Гардасил9», защищающей от инфицирования 9 типами ВПЧ (6, 11, 16, 18, 31, 33, 45, 52, 58). Однако на российском рынке данный продукт ещё не доступен. «Церварикс» зарегистрирована для вакцинации женщин от 10 до 25 лет; «Гардасил» показана к применению детям и подросткам в возрасте от 9 до 15 лет и женщинам от 16 до 45 лет.
Дополнительными факторами риска прогрессирования ПВИ с формированием предраковой патологии являются:
Устранение и профилактика данных факторов способны снизить вероятность развития предраковой патологии шейки матки.
Рак шейки матки поражает преимущественно женщин репродуктивного возраста. Скрининг является важной стратегией вторичной профилактики. Длительный процесс канцерогенной трансформации от появления в организме вируса папилломы человека (ВПЧ) до инвазивного рака дает широкие возможности для выявления заболевания на стадии, когда лечение высокоэффективно. Подходящими скрининговыми тестами в мире признаны цитологическое исследование, визуальный осмотр после применения уксусной кислоты и тесты на выявление ВПЧ. Всемирная организация здравоохранения рекомендует проводить скрининг женщин по крайней мере один раз в жизни в возрасте от 30 до 49 лет. [14]
Согласно приказу Министерства здравоохранения РФ от 03.02.2015. N36ан «Об утверждении порядка проведения диспансеризации определенных групп взрослого населения», осмотр со взятием мазка (соскоба) с поверхности шейки матки и цервикального канала на цитологическое исследование производится 1 раза в 3 года для женщин в возрасте от 21 года до 69 лет включительно.