клетки лейколиза в крови что это значит
Клетки лейколиза в крови что это значит
Диагноз хронического лимфолейкоза (ХЛЛ) может быть установлен при абсолютном количестве лимфоцитов в крови более 5•10 9 /л, наличии в костно-мозговом пунктате не менее 30 % лимфоцитов и иммунологическом подтверждении клонового В-клеточного характера лимфоцитоза.
В подавляющем большинстве случаев предположение о наличии у больного хроническим лимфолейкозом (ХЛЛ) возникает в связи с изменениями картины крови: обнаружение абсолютного и относительного лимфоцитоза. Международное рабочее совещание в 1989 г. установило среди критериев для постановки диагноза хронического лимфолейкоза наличие абсолютного лимфоцитоза в крови не менее 10 • 109/л, однако позже это положение было пересмотрено. В настоящее время для предположения о заболевании ХЛЛ считается достаточным наличие абсолютного лимфоцитоза 5•10 9 /л.
Иногда на протяжении 2—3 лет при числе лейкоцитов, лишь незначительно превышающем норму или даже соответствующем нормальному показателю, наблюдается постепенно нарастающий лимфоцитоз — 50—60—70 %. Эти изменения лейкоцитарной формулы еще не являются оснаванием для постановки диагноза хронического лимфолейкоза без дополнительных исследований: пункции костного мозга и иммунологического исследования крови и костно-мозгового пунктата. Тем не менее такой пациент должен быть под пристальным наблюдением врача: обязательны осмотр и анализы крови каждые 3—4 мес, поскольку, как правило, такие изменения крови являются проявлением начала хронического лимфолейкоза.
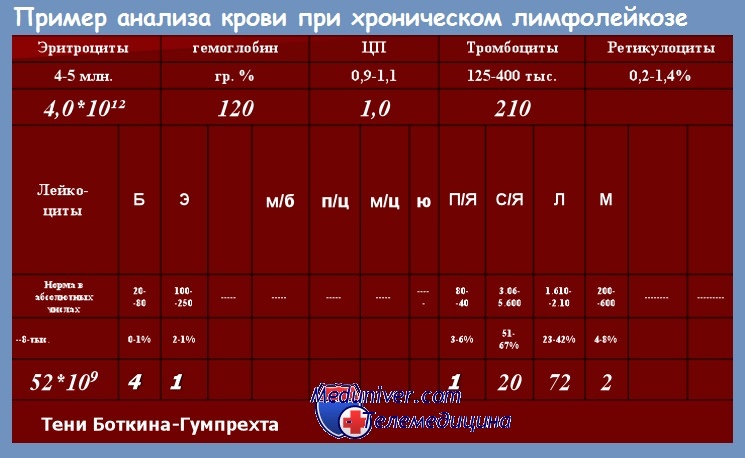
В крови среди ядерных элементов обнаруживается преобладание зрелых лимфоцитов — клеток малого размера, округлых, с плотным ядром и узким ободком светлой или слегка базофильной цитоплазмы. В мазках крови обычно определяется то или иное количество клеток Гумпрехта—Боткина — полуразрушенных размытых ядер лимфоцитов. Их появление связано с повышенной ломкостью мембраны лимфоцитов при хроническом лимфолейкозе.
Количество клеток Гумпрехта — Боткина, как правило, больше у больных с высоким лейкоцитозом. Клетки, или, как их нередко называют, тени Гумпрехта — Боткина, образуются при приготовлении мазка, их наличие и количество не имеют прогностического значения.
Количество лейкоцитов при хроническом лимфолейкозе может быть различным, в большинстве случаев при установлении диагноза хронического лимфолейкоза оно составляет 20—50•10 9 /л, но нередко при первом обращении к врачу уже имеется гиперлейкоцитоз (100—500 • 10 9 /л), свидетельствующий о длительном недиагностированном периоде заболевания. Мы наблюдали больного, у которого при первом обращении к врачу по поводу длительно существующих увеличенных лимфатических узлов количество лейкоцитов оказалось 1200•10 9 /л.
При подсчете лейкоцитарной формулы содержание лимфоцитов обычно составляет 50—70 %, при высоком лейкоцитозе иногда достигает 95—99 %. Наряду со зрелыми лимфоцитами в крови обычно в очень небольшом количестве (как правило, не более 1—3 %) удается обнаружить пролимфоциты — более крупные клетки с отчетливой нуклеолой в ядре. Постепенное увеличение содержания пролимфоцитов в течение болезни, так же как их постоянное присутствие в количестве 10 % и более, является плохим прогностическим признаком.
Е. Matutes и соавт. на большом клиническом материале показали, что выживаемость больных хроническим лимфолейкозом прямо коррелирует с числом циркулирующих пролимфоцитов и значительно снижается уже при числе пролимфоцитов более 5 %.
На основании изучения морфологической картины крови почти 550 больных ХЛЛ Е. Matutes и соавт. выделили примерно 15 % больных с необычной морфологией клеток. Они предложили считать таких больных страдающими атипичным ХЛЛ, отметив два его подтипа: один с повышенным более 10 % количеством пролимфоцитов и второй — с лимфоплазмоцитоидной дифференцировкой лимфоцитов и/или наличием лимфоцитов с расщепленным (cleaved) ядром. Во втором случае одновременно имеются обычные лимфоциты, характерные для хронического лимфолейкоза, и переходные формы — более крупные лимфоциты с выраженной базофилией цитоплазмы или с намечающейся расщелиной ядра.
Течение болезни в этом случае обычно не отличается от характерного для типичного хронического лимфолейкоза, однако нередко при обоих указанных вариантах имеется трисомия хромосомы 12. При обоих подтипах: повышенном количестве пролимфоцитов и лимфоплазмоцитоидной морфологии лимфоцитов — течение болезни у больных с трисомией хромосомы 12 более агрессивное.
Костно-мозговой пунктат при хроническом лимфолейкозе обычно гиперклеточный, инфильтрация лимфоцитами чаще всего имеет диффузный характер, хотя иногда встречаются случаи нодулярной инфильтрации. В большинстве случаев процентное содержание лимфоцитов значительно превышает необходимые для установления диагноза 30 %, нередко достигая 90—95 %.
Лимфоциты в костном мозге морфологически не отличаются от лимфоцитов крови, но обычно имеется 3—5 % пролимфоцитов даже в тех случаях, когда они не обнаруживаются в крови.
При морфологическом исследовании лимфатического узла обнаруживают стирание нормального рисунка и мономорфную инфильтрацию лимфоцитами, морфологически сходными с лимфоцитами крови и костного мозга, иногда имеющими несколько большие размеры. В небольшом количестве встречаются пролимфоциты и клетки, названные параиммунобластами: клетки среднего размера с дисперсным хроматином и круглыми или овальными ядрышками. В селезенке преобладает инфильтрация белой пульпы, хотя красная пульпа обычно тоже оказывается в той или иной степени инфильтрированной малыми лимфоцитами.
Несмотря на характерную картину, результаты морфологического исследования не могут считаться достаточными для установления диагноза хронического лимфолейкоза (ХЛЛ), поскольку аналогичная морфологическая картина крови и костного мозга нередко наблюдается при фолликулярной и мантийно-клеточной лимфомах с поражением костного мозга. Согласно современным критериям, диагноз хронического лимфолейкоза может считаться установленным только после иммунологического исследования, подтверждающего диагноз. Патологические лимфоциты при хроническом лимфолейкозе имеют абсолютно характерный иммунофенотип.
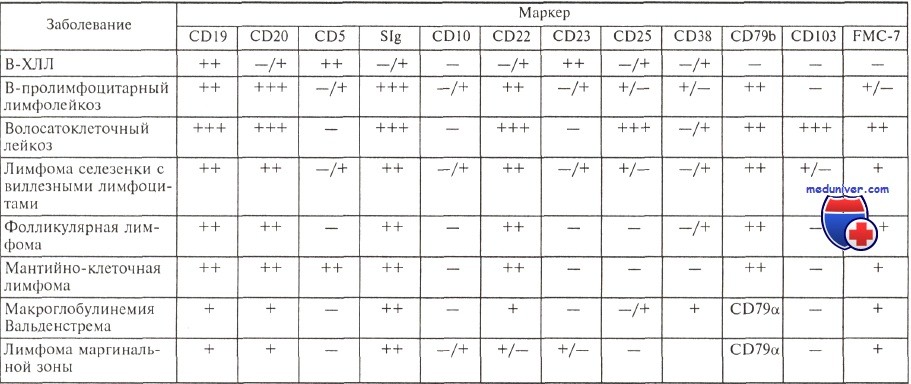
Они экспрессируют антигены CD19, CD5, CD23, отмечается слабая экспрессия на поверхности клеток иммуноглобулинов (экспрессируются IgM, нередко одновременно с IgD) с одной L-цепью, определяется слабая экспрессия антигенов CD20 и CD22, у ряда больных экспрессируется молекула FMC-7. Антиген CD79b, или Igb, являющийся частью В-клеточного рецептора, либо не экспрессируется, либо экспрессируется очень слабо в подавляющем большинстве случаев.
Характерный иммунофенотип опухолевых клеток позволяет отличить В-ХЛЛ от других лимфопролиферативных заболеваний.
Е. Matutes и соавт. предложили числовую систему, помогающую при дифференциальной диагностике В-ХЛЛ и других лимфопролиферативных заболеваний. По этой системе каждый иммунологический признак, характерный для В-ХЛЛ, расценивается как 1 балл, его противоположное значение — как 0.
Иммунофенотип опухолевых клеток при различных лимфопролиферативных заболеваниях
Иногда возникают трудности в дифференциальной диагностике хронического лимфолейкоза и так называемого монокло-нового В-лимфоцитоза неопределенного значения (MLUS — monoclonal lymphocytosis of undetermined significance), названного так по аналогии с моноклоновыми гаммапатиями неопределенного значения (MGUS). Термин был впервые введен еще в конце 80-х годов прошлого века для отличия непрогрессирующего моноклонового лимфоцитоза без признаков ХЛЛ от индолентного ХЛЛ с признаками заболевания. В настоящее время чаще употребляется термин CLUS (clonal lymphocytosis of undetermined significance).
При CLUS обычно на протяжении многих лет сохраняются умеренный и стабильный лейкоцитоз и лимфоцитоз (меньше необходимых для диагноза ХЛЛ 5•10 9 /л), нормальные показатели эритро- и тромбоцитопоэза, отсутствует увеличение лимфатических узлов и селезенки.
В наблюдениях С. Wang и соавт. клиническая картина и лабораторные показатели при CLUS оставались неизменными на протяжении 3—10 лет. Клоновая природа лимфоцитоза была подтверждена рестрикцией L-цепи экспрессируемых на поверхности лимфоцитов иммуноглобулинов. Никаких хромосомных аберраций на протяжении всего времени наблюдения выявлено не было. У всех пациентов исследование иммунофенотипа на протяжении всего времени наблюдения обнаруживало экспрессию лимфоцитами антигенов CD19, CD20 и слабую экспрессию поверхностных иммуноглобулинов, однако неизменно выявляло отсутствие экспрессии CD5 и CD23. Таким образом, данные наблюдения не отвечают всем признакам В-ХЛЛ. Однако в большинстве случаев иммунофенотип при CLUS не отличается от типичного иммунофенотипа В-ХЛЛ. A. Rowstron на основании анализа нескольких сотен наблюдений раннего стабильного хронического лимфолейкоза и сравнения их с CLUS указывает, что частота прогрессирования в этих случаях одинакова и не превышает 10 %.
Известно, что истинный хронический лимфолейкоз, имеющий все необходимые для установления диагноза черты, также может годами не проявлять признаков прогрессирования. В подобных случаях имеется характерный для данного заболевания иммунофенотип, а при длительном наблюдении (в одном нашем наблюдении спустя 22 года со времени постановки диагноза) во многих случаях появляются черты прогрессирующего хронического лимфолейкоза. В других наблюдениях клиническая картина сохраняется неизменной на протяжении всей жизни больного.
Мы наблюдали больную в течение 29 лет, которая не получала никакого лечения, поскольку все это время у нее была стабильная гематологическая и клиническая картина: отсутствие увеличенных лимфатических узлов и селезенки, количество лейкоцитов 15—20•10 9 /л, лимфоцитов 65—70 %. Это наблюдение похоже на наблюдения Т. Han и соавт., описавших 10 больных с лейкоцитозом более 10 • 109/л и моноклоновым В-клеточным лимфоцитозом, у которых в течение 6—24 лет не было признаков прогрессирования и которые не нуждались в терапии.
Возможно, эти наблюдения являются отражением возрастного изменения В-клеточного репертуара. Почти 10 лет назад было обнаружено, что у мышей с возрастом постепенно суживается разнообразие клонов В-клеток (В-клеточный репертуар) и одновременно происходит увеличение размеров (амплификация) отдельных клонов. N. Chiorazzi и М. Ferrarini указывают, что у здоровых людей старше 50 лет наличие таких клонов В-лимфоцитов является обычным. Возможно, отдельные клоны, возникшие под влиянием длительной стимуляции определенным антигеном, могут приобретать значительные размеры и определяться при рутинном иммунологическом исследовании.
Обнаруженная недавно в половине исследованных методом FISH случаев CLUS делеция 13ql4, являющаяся самой частой генетической аберрацией при ХЛЛ, подтверждает мнение о том, что CLUS следует расценивать как раннюю стадию хронического лимфолейкоза доброкачественного течения. В то же время P. Ghia и соавт., обследовав 500 здоровых людей старше 65 лет, обнаружили у части из них клоны клеток с иммунофенотипом, характерным для различных лимфопролиферативных заболеваний, иногда у одного и того же больного. Авторы полагают, что это, скорее всего, является не ранней стадией болезни, а отражением постепенно суживающегося с возрастом В-клеточного репертуара.
В 1982 г. описан постоянный поликлоновый В-лимфоцитоз у курящих женщин средних лет. У некоторых из них были частые респираторные заболевания. Это редкий феномен, и со времени первой публикации появилось не более 90 подобных описаний. Исследования с помощью ПЦР показали, что во всех изученных случаях имеется реаранжировка BCL-2/IgH, которая, однако, не всегда сопровождалась повышенной экспрессией BCL-2.
У некоторых курящих женщин с поликлоновым В-лимфоцитозом обнаружены незначительное увеличение размеров селезенки и поликлоновая гамма-патия, которые, как и лимфоцитоз, иногда исчезали после прекращения курения.
Несколько случаев поликлонового В-лимфоцитоза описаны у некурящих. С помощью ПЦР у некоторых пациентов в крови был обнаружен вирус Эпштейна—Барр. Неясно, играет ли этот вирус роль в развитии синдрома поликлонового В-лимфоцитоза.
Очевидно, в настоящее время подобные случаи не являются трудными для дифференциальной диагностики с хроническим лимфолейкозом (ХЛЛ), поскольку поликлоновый характер лимфоцитоза обнаруживается при иммунофенотипировании. Трудности для трактовки представляет описанный недавно случай поликлонового В-клеточного лимфоцитоза с комплексными хромосомными аберрациями — трисомией хромосом 3, 15 и 18, инверсией хромосомы 18, t(13;14) в отдельных клетках у длительно курящей женщины. Гематологическая картина остается стабильной на протяжении нескольких лет наблюдения, но отмечаются часто повторяющиеся инфекции верхних дыхательных путей. Необходимо длительное наблюдение для выяснения вопроса о том, не являются ли имеющиеся хромосомные аберрации отражением начала лимфопролиферативного заболевания.
При некоторых хронических инфекциях (туберкулез, сифилис), иногда при неинфекционных заболеваниях (тиреотоксикоз, болезнь Аддисона) наблюдается постоянный Т-клеточный лимфоцитоз, чаще всего при нормальном количестве лейкоцитов. Его также нетрудно дифференцировать от хронического лимфолейкоза (ХЛЛ) на основании данных иммунологического исследования.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Хронический лимфоцитарный лейкоз: причины возникновения, симптомы, диагностика, стадии, лечение
Хронический лимфоцитарный лейкоз (ХЛЛ) — это злокачественное заболевание кроветворной ткани, характеризующееся опухолевой трансформацией одного клона лимфоцитов с последующей экспансией им костного мозга, крови, лимфатических узлов и внутренних органов. Злокачественные клетки замещают нормальные, что приводит к дисфункции пораженных органов, расстройствам кровообращения и иммунной защиты.
Одним из первых лабораторных признаков лимфолейкоза является кратное увеличение количества лейкоцитов в периферической крови.
Содержание:
Причины развития хронического лимфолейкоза
К возможным этиологическим факторам развития хронического лимфолейкоза относят:

По мнению ряда ученых, длительная стимуляция иммунной системы человека (например, при частых инфекциях) может приводить к генетическим поломкам и опухолевому перерождению лимфоцитов, образованию клона лейкемических клеток и возникновению ХЛЛ.
Прямой причинной связи между воздействием канцерогенов, ионизирующего излучения и возникновением ХЛЛ не установлено.
Механизм развития хронического лимфолейкоза заключается в преобразовании лимфоцитов в опухолевые клетки и их размножении, что приводит к угнетению нормального кроветворения, развитию анемии и тромбоцитопении.
Симптомы хронического лимфолейкоза
В начальной стадии ХЛЛ пациенты не предъявляют жалоб, их общее состояние удовлетворительное. У некоторых могут проявляться такие неспецифические симптомы как: сильная потливость, быстрая утомляемость, слабость, частые простуды. На данном этапе ХЛЛ выявляется, как правило, случайно на профилактическом осмотре или при обращении к доктору по поводу другого заболевания. Заболевание проявляется абсолютным лимфоцитозом в общем анализе крови и увеличением периферических групп лимфатических узлов (шейных, подмышечные, паховые). Увеличенные лимфоузлы при ХЛЛ пальпаторно мягко — эластичные, безболезненные, не спаяны с окружающими тканями, кожа над ними не изменена.
При медленном течении начальная стадия может длиться несколько лет, при прогрессирующем течении наблюдается быстрое ухудшение общего состояния, значительное увеличение лимфоузлов и селезенки.
Для развернутой стадии ХЛЛ характерна выраженность симптомов. К основным клиническим проявлениям относят:
При этом наблюдаются:
В общем анализе крови — лейкоцитоз (50-200*109/л), лимфоцитоз (до 100*109/л или 80-90 % в лейкоцитарной формуле), анемия и тромбоцитопения, увеличение СОЭ, клеток Боткина — Гумпрехта (разрушенные лимфоциты).
Терминальная стадия ХЛЛ характеризуется:
Диагностика хронического лимфолейкоза
Диагностика хронического лимфоцитарного лейкоза включает в себя сбор анамнеза и уточнение жалоб у пациента, общий осмотр, который заключается в прощупывании периферических лимфатических узлов, печени и селезенки.
Лабораторные методы исследования ХЛЛ
Инструментальные методы исследования ХЛЛ
Также проводятся трепанобиопсия костного мозга и биопсия лимфатических узлов с последующим гистологическим и иммуногистохимическим исследованиями.
Стадии хронического лимфолейкоза
Существует две системы стадирования ХЛЛ, в основы которых положен единый принцип: учет массы опухоли (лимфоцитоз), размеры лимфатических узлов, степень увеличения печени и селезенки, наличие или отсутствие анемии и тромбоцитопении. Совокупность данных фактор влияет на продолжительность жизни и предопределяет прогноз.
Стадии ХЛЛ по европейской классификации Binet
| Стадия | Характеристики | Прогноз | ||
| Анемия HGB | Тромбоциты PLT | Увеличение лимфоузлов | ||
| A | >100 г/л | >100×10 9 /л | в 1-2 областях | хороший |
| B | >100 г/л | >100×10 9 /л | в 3 и более областях | промежуточный 7+ лет |
| C | >100 г/л | >100×10 9 /л | любое количество зон | плохой |
Стадии ХЛЛ по американской классификации RAI
| Стадия | Характеристики | Прогноз | |||
| Лимфоцитоз | Анемия | Тромбоциты PLT | Лимфоузлы увеличены | ||
| 0 в костном мозге: >40% | нет | норма ≥150 x10 9 /л | нет | хороший | |
| I | есть | нет | норма/около нормы | да | относительно хороший |
| II | есть | нет | норма/около сплено/гематомегалия | промежуточный 6+ лет | |
| III | есть | да | норма/около нормы | да/нет | плохой |
| IV | есть | да/нет | 9 /л | да/нет | плохой |
Лечение хронического лимфолейкоза
Течение ХЛЛ неоднородно, поэтому подход к лечению в каждом случае индивидуален и учитывает особенности состояния пациента. Может наблюдаться волнообразный характер течения ХЛЛ с периодами накопления и спонтанной регрессии опухолевого объема. Лечение ХЛЛ подразделяется на специфическую терапию, направленную на подавление клеток опухоли, и симптоматическую терапию.
Показаниями к назначению специфической терапии являются:
Симптоматическая и поддерживающая терапия
Хронический лимфоцитарный лейкоз в настоящее время является неизлечимым заболеванием. Однако своевременное и адекватно назначенное лечение позволяет добиться длительных ремиссий, значительно увеличить продолжительность жизни и улучшить её качество.
ЛЕЙКОЛИЗ
ЛЕЙКОЛИЗ (греч. leukos белый + lysis разрушение, растворение, распад; син. лейкоцитолиз) — растворение, распад, разрушение лейкоцитов. Л. вызывается самыми разнообразными агентами, которые могут привести клетку к гибели.
При Л. клетка теряет свою нормальную структуру, контуры ее становятся расплывчатыми, нередко цитоплазма совсем отсутствует. При лизисе лимфоцитов сохраняются обычно полуразрушенные глыбчатые ядра с остатками ядрышек (нуклеол). Л. нейтрофилов в большинстве случаев приводит к распаду всей клетки; иногда можно видеть разрушение цитоплазмы или только части ее без резких изменений структуры ядра; в других случаях сохраняются лишь остатки ядра и зернистости. При распаде эозинофилов обнаруживаются остатки характерной зернистости, при распаде моноцитов — сетчатая структура ядра и светло-серое облако цитоплазмы. В стадии, предшествующей полному лизису, лейкоциты дистрофически изменяются. Ядра пикнотизируются либо структура их становится разреженной (расплывчатой), может наблюдаться кариорексис, вакуолизация ядра и цитоплазмы.
Разрушенные клетки выявляются в мазках крови после их приготовления. В нормальной крови встречаются единичные разрушенные в результате естественного отмирания клетки. Продолжительность жизни различных лейкоцитов в организме человека исчисляется от нескольких до 100 и более дней. Л. при некоторых заболеваниях, очевидно, связан с изменением физ.-хим. и физиол, свойств клеточных мембран. На проницаемость мембран влияют липиды, которые в виде фосфолипидов и холестерина входят в состав клеточных мембран; возможно, что проницаемость мембран определяется соотношением различных липидных компонентов.
Л. может возникнуть под влиянием токсических веществ различной природы, хим. и физ. агентов, действия ионизирующего излучения, лейкоцитолитической сыворотки и др.
Лизированные клетки обнаруживаются в крови при брюшном и сыпном тифе, при тяжелых инфекциях, орнитозах, малосимптомном инф. лимфоцитозе, остром лейкозе.
Диагностическое значение Л. приобретает при хрон, лимфолейкозе, для к-рого характерны так наз. тени Гумпрехта — разрушенные при приготовлении мазка ядра лимфоцитов с остатками нуклеол. Их число может сильно варьировать, составляя иногда половину всех лейкоцитов крови. Однако показателем тяжести болезни и прогноза лизированные клетки служить не могут.
ЛЕЙКОЛИЗ наблюдается в начальном периоде острого лучевого поражения. Хрон, лучевая болезнь сопровождается небольшим Л.
Л. возникает в случаях незавершенного фагоцитоза, когда поглощенные лейкоцитами микробы не подвергаются перевариванию, сохраняются и размножаются в клетке. Лимфадениты, вызванные банальной инфекцией, могут сопровождаться значительным Л. Реже Л. отмечается при фагоцитозе лейкоцитами гонококков. Сроки распада лейкоцитов в ряде случаев определяются циклом развития возбудителя в лейкоцитах, как, напр., при орнитозах.
Библиография: Даштаянц Г. А. и Вайсман С. Г. Лейколиз — новый лабораторный тест для определения активности ревматического процесса, Врач, дело, № 7, с. 36, 1971; Федоров И. И. и др. К методике определения лейколиз а в крови, Лаборат, дело, Ne 5, с. 268, 1971.
Как распознать лейкоз по анализу крови?
Врач-гематолог, доктор медицинских наук Сергей Семочкин про острый лимфобластный лейкоз
Врач-гематолог, профессор кафедры онкологии, гематологии и лучевой терапии РНИМУ им. Н. И. Пирогова Минздрава России, доктор медицинских наук Сергей Семочкин рассказал: можно ли распознать острый лимфобластный лейкоз (ОЛЛ) на ранней стадии и поставить диагноз по анализу крови; объяснил, как лечат ОЛЛ и кому показана трансплантация костного мозга (ТКМ).
Каковы ранние симптомы острого лимфобластного лейкоза? Можно ли их увидеть и распознать ОЛЛ?
В данном случае все достаточно просто, потому что слово «острый» означает, что заболевание внезапное и зачастую симптомы очень выразительные. Самый частый симптом — это лихорадка, т.е. повышение температуры тела. Лихорадка может быть как субфебрильной, так и ярко выраженной, до 39 градусов. Появятся изменения, связанные с поражением костного мозга. Снижение гемоглобина приведет к слабости и быстрой утомляемости. Могут увеличиться лимфатические узлы, появиться дискомфорт в брюшной полости за счет того, что увеличиваются размеры печени и селезенки. Могут быть проявления кровоточивости — даже во время чистки зубов. У некоторых пациентов ОЛЛ может начаться с неврологических проявлений – головных болей, головокружения и прочих проблем. Симптоматика обширная, но в данном случае она является достаточно острой, внезапно возникшей.
Можно ли поставить диагноз по анализу крови? Что он покажет?
Как правило, в анализе крови есть ярко выраженные показатели: изменены ростки кроветворения, количество лейкоцитов выходит за пределы нормы — может упасть ниже нормальных значений, а может стать запредельно огромным. Мне встречались пациенты, у которых количество лейкоцитов при норме от 4 до 9 тысяч повышалось до 200 тысяч на мкл. Тромбоциты тоже в ряде случаев очень сильно снижены, но главное – изменение количества лейкоцитов. Очень важным маркером является выход опухолевых клеток в кровь, когда в крови появляются незрелые ранние клетки, которые называют бластными. Если в анализе крови выявили бластные клетки, то это, скорее всего, либо острый лейкоз, либо миелодиспластический синдром.
Как пациент попадает к гематологу?
Анализ крови с характерными изменениями — повод для немедленного вызова скорой помощи и госпитализации пациента в профильный стационар. При лечении детей и подростков у онкогематолога, как правило, есть один-два дня ни диагностику, лечение необходимо начинать, как можно раньше. В диагностику входит повторный анализ крови, затем – верификация диагноза, для которой проводят биопсию костного мозга. У маленьких детей ее проводят под общей анестезией, у взрослых — под местной. С помощь небольшой иглы делаю прокол грудины или подвздошной кости. У детей пункцию грудины не делают. Полученный образец костного мозга, который выглядит как обычная пробирка с кровью, отправят в лабораторию, где для подтверждения диагноза проведут целый спектр исследований. Главный критерий – увеличение количества бластных клеток. Только по внешнему виду и по количеству бластных клеток определить вариант лейкоза – невозможно. Еще в 1913 году установили, что есть лимфоидный, а есть миелоидный вариант лейкоза. Для верификации применяются специальные лабораторные методы: иммунологические и химические. Существует специальный прибор – проточный цитометр, с помощью которого определяют маркеры, характеризующие данный тип клеток. Для определения подвида острого лейкоза, применяют целый спектр генетических исследований, чтобы выйти на более целевую терапию у этих пациентов.
Каковы причины возникновения ОЛЛ? Существует мнение, что этот вид лейкоза очень сильно взаимосвязан с экологическими проблемами, передается по наследству и часто возникает у тех, кто уже переболел каким-то онкологическим заболеванием. Правда это или нет?
Истинную причину возникновения лейкоза у взрослых можно выявить только в 5% случаев, в 95% совершенно непонятно, что там к чему привело. У детей все несколько интересней.
Как возникает лейкоз? В генетическом материале клетки возникает некая первичная мутация, которая сама по себе далеко не всегда приводит к лейкозу. В дальнейшем к этой мутации присоединяются другие, и когда болезнь все же возникает, в клетке накоплено уже много молекулярных событий, сочетание которых привело возникновению заболевания. Пик острого лимфобластного лейкоза приходится на детей от двух до четырех лет, потом заболеваемость падает. Следующий пик приходится на 18-29 лет, потом снова спад. После 60 лет — опять небольшой рост.
У части детей раннего возраста прослеживается некая врожденная составляющая этой проблемы. Встречаются случаи ОЛЛ у плода или новорожденного, когда ребенок рождается уже с заболеванием, либо заболевает в течение первого года жизни. Исследования пуповинной крови показали, что у новорожденных встречаются лейкемические поломки, врожденные мутации, которые могут привести к возникновению лейкоза. И мутацию эту вызывает наследственный фактор, сработавший во время внутриутробного развития. По разным данным, общее количество таких младенцев составляет от 1 до 5%. Дальше многое зависит от инфекционной обстановки, сложившейся вокруг ребенка. Многочисленные инфекции, перенесенные в детстве, способствуют формированию нормальной иммунной системы, которая нейтрализует наследственный фактор.
Если говорить про экологические проблемы, то с ними четкой связи не выявлено.
Влияет ли УФ-излучение, СВЧ, солнечные лучи, радиация?
В Хиросиме и Нагасаки повышенная заболеваемость держалась около 12 лет. После Чернобыля у многих пострадала щитовидная железа, но заболеваемость лейкозами не выросла. Все зависит от типа изотопов попавших в окружающую среду. В Фукусиме тоже этого не случилось, потому что концентрация радиоактивных веществ сильно разбавилась морской водой.
Вред ультрафиолета научно доказан только в отношении меланомы. Четкой связи с ОЛЛ нет. Своим бывшим пациентам мы не разрешаем посещать солярий и не рекомендуем загорать, потому что хотя связь и не доказана, совсем исключать этот фактор тоже нельзя.
Если говорить об СВЧ-излучении, домашние микроволновые печи абсолютно безопасны.
Как лечат ОЛЛ? Что ждет пациента?
Концепция лечения ОЛЛ, которая до сих поре лежит в основе протоколов лечения ОЛЛ, была разработана американским педиатром Дональдом Пинкелем еще в 1962 году. Она включает в себя четыре этапа: индукция ремиссии, консолидация, воздействие на центральную нервную систему и длительный этап поддерживающей терапии на протяжении двух-трех лет. Во всем мире проводится лечение по клиническим протоколам, разработанным в результате кооперированных исследований. Согласно некоторым работам, строгое следование протоколам повышает выживаемость пациентов на 15-20% по сравнению с индивидуализированным лечением. В протоколе прописаны все действия: от первого дня до последнего. В нем есть указания, как и в какой момент оценивать возникающие осложнение и что с ними делать. В России два центра, активно ведущих такие протоколы. Центр им. Дмитрия Рогачева, где Александр Исаакович Карачунский в течение многих лет, с начала 1990-х, ведет серию протоколов «Москва — Берлин». Каждые пять лет дизайн протоколов пересматривают, чтобы улучшить лечение отдельных категорий пациентов. уже в течение многих лет с начала 90-х годов серию протоколов Москва-Берлин. Каждые пять лет меняется дизайн протоколов, направленных на улучшение лечения отдельных категорий пациентов. Во взрослой практике — это НМИЦ гематологии, где ведут кооперированные исследования по острому лимфобластному лейкозу у взрослых.
В каких случаях показана трансплантация костного мозга (ТКМ)?
В отличие от острого миелоидного лейкоза, показаний к аллогенной (от донора) ТКМ меньше. Ее назначают пациентам, которые не достигли ремиссии в указанные протоколом сроки или имеют неблагоприятный цитогенетический вариант заболевания. В детской практике выздоравливают более 90% детей, и примерно 15-20% являются кандидатами для аллогенной ТКМ. У взрослых процент пациентов нуждающихся в трансплантации несколько выше, за счет того, что генетических операций высокого риска становится намного больше и ответ на стандартное лечение хуже. Когда мы обсуждали хронический миелолейкоз, там фигурировала филадельфийская хромосома — транслокация (9;22). При ОЛЛ это абсолютно негативный фактор прогноза. У детей такая мутация встречается меньше чем в 5% случаев, у людей старше 50-60 лет примерно половина В-линейных ОЛЛ будет с филадельфийской хромосомой. В отличие от хронического миелолейкоза, применение ингибиторов тирозинкиназы при остром лимфобластном лейкозе не столь успешно. Вот поэтому во взрослой практике ТКМ необходимо проводить примерно 30% пациентов. Возрастной порог для аллогенной ТКМ — в районе 55 лет, это разумно.
Как часто случаются рецидивы с ОЛЛ?
Если мы говорим про взрослых людей, то рецидивы случаются почти в 40% случаев. Бывают ранние рецидивы, которые случаются прямо на терапии. В таком случае необходимо менять лечение, делать его более интенсивным и тяжелым. В таких случаях, как правило, показана ТКМ. Поздний рецидив может случиться и через 20 лет. К сожалению мы не можем убрать причину, которая вызывает это заболевание — оно может вернуться.
Можно ли планировать беременность после ОЛЛ?
Длительная химиотерапия нарушает фертильность, поэтому лучше провести криоконсервацию спермы/яйцеклетки, а еще лучше эмбриона — это более надежный способ. У мужчин, как правило, серьезно нарушается сперматогенез, но у женщин дело обстоит несколько лучше. Вероятность забеременеть и выносить здорового ребенка высока. Если прошло не менее пяти лет в ремиссии, никаких ограничений нет.
Может ли беременность быть провоцирующим фактором для рецидива?
Скорее, нет. Это не такое частое явление, как при некоторых других заболеваниях, где беременность действительно может стать провоцирующим фактором.
Передается ли ОЛЛ по наследству?
Лимфобластный лейкоз – редкое заболевание, поэтому вероятность того, что он случится у ребенка, рожденного от родителей после ОЛЛ, крайне мала.
Как будут лечить ОЛЛ в будущем?
Представляется, что в основе лечения онкологических заболеваний в будущем станет активация собственного иммунитета. Нам необходимо настроить иммунную систему таким образом, чтобы она распознавала и убирала раковые клетки. Сейчас мы находимся на раннем этапе развития CAR-T-терапии, но через какое-то время технологии настолько усовершенствуются, что, скорее всего, она станет одним из основных методов терапии при целом ряде онкогематологических заболеваний. Суть метода заключается в том, что у пациента собирают его собственные Т-лимфоциты и отправляют в специальную лабораторию. Эта лаборатория может быть в другом городе, стране — не важно. В лаборатории эти Т-лимфоциты перепрограммируются: в них появляется информация об опухолевых клетках, присутствующих в организме пациента. После перепрограммирования Т-лимфоциты вводят обратно пациенту, она находят раковые клетки и возникает ремиссия. Основные проблемы – создать качественный процесс распознавания и разработать стандартные протоколы лечения.
Много вопросов возникает в понимания биологии заболевания, потому как каждый конкретный случай весьма индивидуален. Мы знакомы только с грубыми поломками, но каждая отдельная поломка провоцирует различное течение болезни. Мы уже сейчас можем полностью секвенировать геном опухолевой клетки и главное научиться понимать, что в патогенезе является ключевым и как на это можно воздействовать, тогда мы ближе подойдем к полному излечению болезни. За этим будущее.