депозиты в медицине что это
Стадии рака: классификация онкологических заболеваний
Стадия онкологического заболевания дает информацию о том, насколько велика опухоль и распространилась ли она по организму. Это помогает врачам определять прогноз пациента и план лечения.
С помощью врача-онколога, резидента Высшей школы онкологии Сергея Югая разбираемся, как врачи устанавливают стадии рака и что каждая из них означает.
На что влияет стадия онкологического заболевания?
Стадирование нужно, чтобы спрогнозировать, какие у пациента шансы на выздоровление, а также чтобы определить, какой метод лечения будет наиболее эффективен в конкретном случае, — поясняет Сергей Югай.
Все начинается с медицинского осмотра и обследований — УЗИ, КТ, МРТ, ПЭТ-КТ и других методов в зависимости от вида рака. Затем врач берет кусочек опухоли — биопсию или удаляет опухоль целиком во время операции, а после отправляет материал на гистологический анализ, чтобы поставить диагноз.
Стадии рака по TNM-классификации
Стадии онкологического процесса описывают разными способами — это зависит от вида опухоли. Один из самых распространенных способов — стадирование с помощью TNM-классификации.
Т характеризует первичную опухоль, ее размеры и вовлечение окружающих структур в опухолевый рост, например, прорастание в стенку кишки или желудка. N говорит о наличии в лимфоузлах метастазов и количестве пораженных лимфоузлов, а М — о наличии отдаленных метастазов (во внутренних органах, костях, ЦНС или лимфоузлах, которые расположены далеко от первичной опухоли), — объясняет Сергей Югай.
Индекс Т принимает значения от 0 до 4. 0 означает, что первичная опухоль не обнаружена, 1 — опухоль маленькая, а 4 — опухоль проросла в прилегающие ткани. Таким образом, чем больше цифра рядом с Т, тем ситуация сложнее. При некоторых видах рака N принимает значение 0 или 1, при других — 0, 1 или 2, а иногда — 0, 1, 2 и 3. 0 означает, что опухоль не проникла в ближайшие лимфоузлы, а 3 — что поражено множество лимфоузлов. M0 показывает, что метастазов нет, а 1 — что метастазы есть.
Онкологи выставляют стадию по TNM клинически — до операции или когда операция не планируется и патоморфологически — при изучении удаленной во время операции опухоли, — объясняет Сергей.
Клиническая стадия обозначается буквой «c», например, cT2. Патоморфологическая — буквой «p», например, pN1.
От правильной стадии зависит тактика лечения. Например, пациент — мужчина с раком желудка и стадией cT1N0M0. Это значит, что опухоль прорастает в слизистую и подслизистый слой стенки желудка. В этом случае пациенту показана операция. Если же стадия выше (cT2N1M0, например), то есть опухоль пациента прорастает в мышечный слой, и есть метастазы в лимфоузлах, то может понадобиться химиотерапия перед операцией, которая позволит улучшить результаты лечения, — добавляет Сергей.
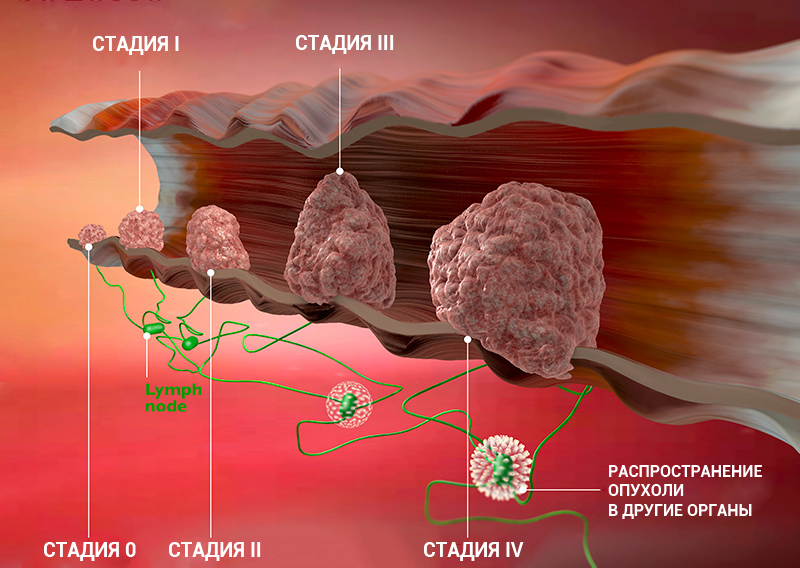
Стадию рака могут обозначать с помощью цифр — 0, I, II, III, IV. Что это значит?
Клинические стадии (0, I, II, III, IV) тесно связаны с системой TNM. Как правило, одна клиническая стадия включает в себя несколько вариантов стадирования по TNM. Эти варианты характеризуются схожими прогнозом и подходом к лечению. Например, стадии T1N3M0, T2N3M0, T3N2M0 рака легкого объединяются в IIIВ стадию, так как при любой из этих ситуаций пациент будет иметь примерно одинаковый прогноз и тактику лечения. В этом конкретном примере необходима химиолучевая терапия, а не операция, — комментирует Сергей Югай.
Меняется ли стадия после лечения, при прогрессировании заболевания?
Нет, стадия выставляется один раз. Но есть нюансы:
Например, мы хотим посмотреть, как опухоль ответила на лечение, чтобы понять, можно ли делать операцию. После лечения опухоль уменьшилась, и мы добавляем к стадии новые данные. При прогрессировании опухолевого процесса первоначальная стадия также остается прежней, но, к сожалению, прогноз будет менее благоприятный. Например, у человека II стадия рака желудка. Он прооперирован, и прогноз у него хороший. Через 2 года врачи обнаруживают у пациента метастазы в легких. Стадия остается II, но рак у пациента уже метастатический, что очень усложняет положение, — говорит Сергей.
Бывает, что люди сравнивают свою ситуацию с историями других пациентов. Если речь идет о разных онкологических заболеваниях, то такие сравнения некорректны — это заболевания с разными прогнозами и схемами лечения:
Например, с нейроэндокринным раком поджелудочной железы люди могут жить десятилетиями, а при метастатической стадии рака поджелудочной железы — полгода или год, — объясняет врач-онколог.
Что может повлиять на прогноз людей с одинаковой стадией и одним видом рака?
Сергей Югай выделяет три фактора:
Метастазы в костях
Какие злокачественные заболевания осложняются
метастазами в костях
Какие кости поражаются при раке
Принципиально возможно развитие метастаза в любой кости скелета, но чаще всего опухолевые клетки задерживаются в костях с лучшим кровоснабжением, где всегда есть достаточное питание для продолжения неуправляемого деления. Очень редко метастазы образуются в мелких косточках кисти и стопы, но часты в обильно пронизанных сосудистой сетью костях таза, позвонках и ребрах, нередко поражают кости черепа, за исключением лицевого скелета. Наибольшую опасность для пациента несёт опухолевое поражение позвонков и трубчатых костей конечностей, когда в месте деструкции при обычной нагрузке случается перелом, лишающий возможности двигаться, а при патологическом переломе шейного позвонка высока вероятность паралича из-за сдавления спинного мозга отломками разрушенной опухолью кости.



Какими бывают метастазы в костях
Раковые клетки разрушают ткань кости, вызывая её деструкцию, которая может проявляться как разрежением костной ткани с образованием бескостных участков, так и увеличением патологической, гораздо менее прочной и чётко структурированной костной массы.
По распространённости выделяют:
Диагностика метастазов в костях
До «эры визуализации» деструктивные изменения скелета выявляли при рентгенологическом обследовании и остеосцинтиграфии – изотопном исследовании. Остеосцинтиграфия очень чувствительна, она обнаруживает крохотные опухолевые образования, не видимые на рентгенограммах, поэтому и сегодня она актуальна и обязательна для каждого онкологического пациента.
Рентгенография способна обнаружить очаг более сантиметра, КТ высокочувствительна, но уступает МРТ при необходимости параллельной визуализации прилежащих к кости мягких тканей и суставов. Наилучшая диагностика – ПЭТ и МРТ или КТ. Остеосцинтиграфия признана стандартным методом скрининга – диагностика для 100% больных раком, по местам накопления изотопа в виде «горячих точек» выполняется прицельное рентгенологическое или визуализирующее исследование – МРТ или КТ.
Динамическое наблюдение за течением метастазирования и оценка результатов лечения должны осуществляться одним способом, на одном аппарате и, желательно, одним и тем же специалистом. Если до начала терапии не удалось выполнить МРТ, а было сделано только КТ, то и оценивать итоги терапии надо по КТ
Клинические проявления метастазов в кости
В начальной стадии костное метастазирование проявляется болевым синдромом только у каждого шестого онкологического больного, у абсолютного большинства вначале процесса нет никаких признаков. Боль появляется при проникновении раковых клеток в обильно иннервированную покровную костную ткань – надкостницу, внутри кости нервных окончаний почти нет, поэтому и боли не бывает.
Считается, что остеолитические очаги чаще вызывают боли, а остеопластические протекают без симптомов, но могут проявляться выбуханием – «наростом» в месте поражения.
Неблагоприятное осложнение опухолевого поражение кости – патологический перелом в месте деструкции:
Химиотерапия при метастазах в костях
Преимущественно при костных поражениях используют лекарственный метод – химиотерапию или гормонотерапию, для минимизации возможных осложнений в виде переломов и повышения концентрации кальция в крови дополнительно вводят бисфосфонаты. Бисфосфонаты помогают уменьшить болевой синдром.
Химиотерапия проводится длительно, частые контрольные обследования нецелесообразны, поскольку костная ткань на месте уничтоженной опухоли растет очень медленно. Практически всегда при химиотерапии достигается хороший обезболивающий эффект. При интенсивном болевом синдроме зону деструкции можно облучить, в обязательном порядке лучевой терапии подлежит метастазирование в шейные позвонки, что снижает вероятность перелома.
Операция при метастазах в костях
Хирургическое лечение при метастазировании в скелет преследует одну из двух целей:
Радикальное лечение возможно при отсутствии первичного рака и одиночном метастатическом поражении скелета. После стабилизации роста солитарного – единственного костного метастаза, с помощью курсов химиотерапии, ставится вопрос об оперативном лечении. Как правило, таким способом лечат поражения конечностей.
Сегодня есть возможность заменить протезом пораженные кости верхних и нижних конечностей, но чаще к операции прибегают при патологическом переломе, когда из-за обширной опухолевой деструкции маловероятно восстановление костной целостности. Операция сложная, требующая плановой подготовки, в том числе и нескольких предварительных курсов химиотерапии и долгого лекарственного лечения после операции.
Такие вмешательства выполняются специальной бригадой, владеющей навыками онкологов и травматологов-ортопедов, в специальной операционной, оснащенной рентгеновским оборудованием, но лучше – КТ-установкой. Опухоль разрушает не только кость, но и прорастает в окружающие мягкие ткани – мышцы, сухожилия и суставы, очень важно для будущего восстановления удалить всё поражённое раком, поэтому во время оперативного вмешательства возникает необходимость уточнения объективной реальности с помощью высокоточной КТ.
Депозиты в медицине что это
аутоТГСК — трансплантация аутологичных гемопоэтических стволовых клеток крови
БДЛЦ — болезнь депозитов легких цепей
МГПП — моноклональная гаммапатия с преимущественным поражением почек
ММ — множественная миелома
ОхЧР — очень хорошая частичная ремиссия
ПН — почечная недостаточность
ПР — полная гематологическая ремиссия
СКФ — скорость клубочковой фильтрации
ХБП — хроническая болезнь почек
ЧР — частичная ремиссия
Болезнь депозитов легких цепей (БДЛЦ) — редкое системное заболевание, характеризующееся отложением моноклональных легких цепей (ЛЦ) в различных органах, что приводит к прогрессирующему нарушению их функции. БДЛЦ может быть ассоциирована с лимфопролиферативными заболеваниями: в 20% случаев выявляют множественную миелому (ММ), значительно реже — макроглобулинемию Вальденстрема, другие индолентные лимфомы [1]. В большинстве случаев БДЛЦ признаки гемобластоза или лимфомы отсутствуют. Для обозначения заболеваний, вызванных секретируемым парапротеином, но не пролиферацией опухолевых клеток, предложен термин «моноклональная гаммапатия с преимущественным поражением почек» (МГПП) или monoclonal gammopathy of renal significance—MGRS), объединяющий AL-амилоидоз, БДЛЦ, иммунотактоидную нефропатию, моноклональный криоглобулинемический гломерулонефрит и другие варианты поражений почек [2].
При БДЛЦ в 70—80% случаев выявляют секрецию моноклональных ЛЦ κ [3—6]. Количество моноклональных ЛЦ в сыворотке при БДЛЦ значительно меньше, чем при каст-нефропатии (КН), и, как правило, составляет 500 — 1500 мг/л [6, 7]. В 15—20% случаев выявить секрецию моноклональных ЛЦ не удается.
Основным проявлением БДЛЦ служит нефропатия. В 35% случаев наблюдается вовлечение других органов, главным образом, сердца и печени. Описано также отложение моноклональных иммуноглобулинов в периферических нервах, лимфатических узлах, головном мозге, селезенке, кишечнике, надпочечниках, сосудах, легких, коже [8—11].
Диагноз БДЛЦ можно установить только на основании морфологического исследования биоптата пораженного органа (чаще почки) с применением световой, иммунофлюоресцентной и иногда электронной микроскопии. При исследовании биоптата почки методом световой микроскопии при БДЛЦ выявляется характерный нодулярный гломерулосклероз [4, 12]. Клубочки имеют узловатый вид за счет неравномерного увеличения мезангиального матрикса с различной степенью его клеточности. В базальных мембранах и внеклеточном матриксе обнаруживают гомогенный, негативный при окрашивании конго-красным, PAS-позитивный материал с мелкозернистой ультраструктурой. Основной локализацией депозитов ЛЦ являются базальные мембраны канальцев и капилляров клубочков, в меньшей степени — мезангиальный матрикс, базальные мембраны гладкомышечных стенок артерий и интерстициальная ткань. Вместе с тем многие исследователи отмечают гетерогенность изменений при световой микроскопии. В ряде случаев клубочки могут выглядеть неизмененными или отмечается небольшое расширение мезангия. В 32% случаев БДЛЦ изменений при световой микроскопии не выявлено [13].
Наиболее информативным методом исследования в диагностике нефропатии вследствие БДЛЦ является иммунофлюоресцентное исследование биоптата почки. Диагноз считают подтвержденным при обнаружении линейно расположенных депозитов вдоль базальной мембраны канальцев и/или клубочков, содержащих моноклональные ЛЦ одного типа (чаще κ). Реже депозиты выявляют в других структурах нефрона: в мезангии (83%), интерстициальной ткани (30%), артериолах (65%) [3, 5].
При электронной микроскопии выявляют гранулярные электронно-плотные депозиты, расположенные в базальной мембране клубочков, канальцев, стенках артерий, мезангиальном матриксе и интерстициальной ткани. В базальной мембране клубочков мелкогранулярный электронно-плотный материал локализуется преимущественно субэндотелиально, при локализации в канальцевой базальной мембране — вдоль наружной ее части, обращенной к интерстициальной ткани.
Нефропатия вследствие БДЛЦ проявляется клубочковой протеинурией, микрогематурией, характерна артериальная гипертония, примерно в половине случаев развивается нефротический синдром. Почечную недостаточность (ПН) выявляют в момент диагностики у 96% пациентов. В среднем через 2 года от начала заболевания у 57% развивается уремия, при которой требуется лечение программным гемодиализом (ГД) [3].
При исследовании биоптатов почек лишь у 2—8% больных ММ выявляют БДЛЦ [6, 14, 15]. Чаще (в 15— 27% случаев) выявляют сочетанное поражение в виде БДЛЦ и К.Н. При сочетанном поражении почек нефротический синдром отсутствует, часто в дебюте заболевания развивается зависимая от диализа П.Н. При световой микроскопии нодулярный гломерулосклероз выявляют значительно реже — лишь в 18% случаев. Клубочки могут выглядеть неизмененными, иногда обнаруживают умеренное расширение мезангия [15, 16].
Терапия БДЛЦ направлена на эрадикацию клона плазматических клеток. При легкой и умеренной ПН (скорость клубочковой фильтрации — СКФ более 30 мл/мин) в результате успешного лечения возможно сохранение или улучшение функции почек. При тяжелой ПН (СКФ 
В результате терапии по программе VCD у 4 пациентов получена ПР, у 3 — ОхЧР. В связи с неэффективностью 2 больных переведены на терапию второй линии, включающую леналидомид и дексаметазон (Rd), что позволило достигнуть ПР и частичной ремиссии (ЧР). После завершения индукционной терапии в 2 случаях выполнена высокодозная ХТ с аутоТГСК. Несмотря на достижение гематологического ответа у всех больных, функция почек улучшилась лишь у 2 (табл. 2).

Обсуждение
Диагноз БДЛЦ основан на морфологическом исследовании биоптата пораженных органов, в основном почек, что сопряжено с необходимостью выполнения пункционной биопсии и связанным с этим риском развития геморрагических осложнений. Во всех представленных случаях поражение почек было основным синдромом заболевания, что послужило основанием для госпитализации пациентов в нефрологическую клинику. Впервые выявленная ПН неясной природы явилась показанием к выполнению биопсии почки, что позволило диагностировать БДЛЦ.
Нефропатия вследствие БДЛЦ — показание к углубленному гематологическому обследованию для уточнения выраженности плазматической инфильтрации костного мозга, показателей моноклональной секреции, а также для исключения опухолевых заболеваний системы крови. Наш небольшой опыт показал, что у большинства больных при тщательном диагностическом поиске, включающем цитологическое, гистологическое, а также иммуногистохимическое исследование костного мозга, низкодозовую компьютерную томографию всех костей скелета, доказана М.М. Лишь у 3 пациентов признаки опухолевого заболевания не обнаружены, на основании чего БДЛЦ рассматривалась в рамках МГПП. Обращает внимание, что ММ с БДЛЦ (без сопутствующей КН) характеризуется небольшой опухолевой массой (I стадия по классификации Durie—Salmon, 1975 г.) и соответственно отсутствуют такие симптомы ММ, как оссалгии, гиперкальциемия, мягкотканные образования. Эти наблюдения подтверждают, что симптомы заболевания в большей степени определяются повреждением органов секретируемым парапротеином, чем пролиферацией плазматических клеток и опухолевой массой.
Независимо от того, ассоциирована ли БДЛЦ с ММ или нет, терапия направлена на редукцию моноклональной секреции и основывается на принципах терапии М.М. Лечение по схемам, содержащим бортезомиб, позволило достигнуть гематологического ответа у 7 из 9 пациентов, в остальных 2 случаях оказалась эффективной терапия второго ряда с леналидомидом. У 2 пациентов использована высокодозная ХТ с мелфаланом с последующей аутоТГСК. Несмотря на то что у 8 из 9 больных достигнута высокая степень гематологического ответа (у 5 пациентов ПР, у 3 ОхЧР), улучшение функции почек отмечено лишь в 2 случаях. Столь низкая частота «почечного» ответа обусловлена тем, что у большинства больных лечение начато поздно — в IV и V стадиях ХБП.
Заключение
Следует обратить внимание специалистов на эту патологию, которую с широким внедрением в нефрологическую практику метода пункционной биопсии почки стали выявлять все чаще. Современные программы терапии позволяют эффективно редуцировать моноклональную секрецию у большинства больных. Однако лишь при своевременно начатом лечении возможно сохранить функцию пораженных органов и существенно продлить жизнь пациентам.
Что нужно знать о метастатическом раке груди в кости
Костные метастазы рака груди — это вторичные злокачественные очаги. Они возникают в костной ткани после попадания в нее опухолевых клеток молочной железы. Такому онкологическому заболеванию всегда присваивается четвертая стадия по степени тяжести.
Причины метастазов рака груди
Раковые опухоли груди — вторая по частоте встречаемости онкопатология у женщин. Изредка это заболевание поражает и мужчин. В молочной железе оно способно давать метастазы — отдельные опухолевые клетки, которые отрываются от первичного очага и с током крови или лимфы переносятся в другие, иногда достаточно отдаленные, органы и ткани. Там они оседают и дают рост вторичным опухолевым очагам.
Рак молочных желез наиболее часто метастазирует в:
При этом костная ткань — наиболее частая мишень для распространения метастазов из опухолей груди. Примерно 80% всех костных метастазов происходят из молочных желез, а также из раковых опухолей предстательной железы и легких. Конкретная локализация вторичных очагов в костях может быть различной. Однако они образуются преимущественно в:
Высокая частота распространения метастазов в кости обусловлена тем, что костная система постоянно подвергается ремоделированию. Старые ткани постепенно отмирают и заменяются новыми на протяжении всей жизни человека. Опухолевые клетки, попадая в эту динамическую биологическую среду с хорошим кровоснабжением, быстро начинают активный рост. В зависимости от конкретной зоны кости, где развился вторичный опухолевый очаг, он может приводить к разрушению костных структур или к патологическому перепроизводству ткани.
Симптомы костных метастазов
Обычно первыми проявлениями этой патологии становятся внезапные переломы, возникающие при очень слабых физических воздействиях. Если опухоль сдавливает нервные пути, проходящие рядом с костями, это может вызывать локальную болезненность или нарушения чувствительности. Тип и тяжесть симптоматики может меняться в зависимости от того, где именно возникла метастатическая опухоль и какие размеры она имеет.
Иногда метастазы в костях обнаруживают еще до того, как будет поставлен диагноз. Однако вторичные костные очаги могут выявлять и через несколько лет после успешного лечения рака молочных желез.
Диагностика костных метастазов
Для обнаружения метастазов используют различные методы визуализации:
Из лабораторных исследований значение имеет анализ крови. В нем может наблюдаться увеличение концентрации кальция и щелочной фосфатазы. Наконец, используется пункционная биопсия. Взятый материал отправляют на гистологическое исследование, которое и устанавливает окончательный диагноз.
Лечение костных метастазов
К сожалению, вторичные опухолевые очаги в костях очень плохо поддаются лечению. Обычно основные усилия врачей направлены на замедление роста опухоли, а также улучшение состояния пациента при помощи паллиативной терапии. Используемые препараты позволяют:
Кроме того, в некоторых случаях показаны лучевое лечение метастазов, гормональная терапия и проведение хирургических вмешательств.
Прогноз при метастатическом раке костей
Вторичные опухолевые очаги в костях обычно имеют неблагоприятный прогноз. Однако некоторые люди после постановки такого диагноза продолжают жить полноценной жизнью. Ее качество для пациента будет зависеть от ряда факторов, основные из которых — это:
Некоторые исследования показывают, что средняя годовая выживаемость людей с метастатическим раком костей составляет 40–60%. Так, исследование, проведенное в 2017 году в Дании, продемонстрировало, что годовая выживаемость среди людей с метастатическим раком костей немного выше, если источником заболевания является рак груди, а не простаты или легких. Среднюю выживаемость таких пациентов ученые определили в промежутке между 12 и 33 месяцами после обнаружения метастазов в костной ткани.
Лечение костных метастазов рака груди в Турции
Врачи турецкой клиники «Анадолу» проводят диагностику и лечение злокачественных опухолей молочной железы и их метастазов в соответствии со строгими мировыми стандартами. Здесь используется наиболее современное оборудование и лечебные методики, врачи широко применяют:
Для лечения костных метастазов онкологи «Анадолу» используют высокоточные методы диагностики, гормонотерапию, химиотерапию в соответствии с протоколами, утвержденными ВОЗ, лечение при помощи установки КиберНож и других современных методов лучевой терапии.
Психологическая поддержка
Онкологическое заболевание — это всегда серьезная стрессовая ситуация, связанная с сильным негативным эмоциональным потрясением. Человека, который столкнулся с этим заболеванием, должны окружать его родные и близкие, оказывать ему всестороннюю поддержку. Кроме того, важна и профессиональная психологическая помощь, получить которую можно в специальных группах и у специалистов в форме консультирования. Главное, чтобы человек не оставался со своим заболеванием один на один. Врачи «Анадолу» прекрасно знают о важности психологической поддержки, поэтому пациент всегда может рассчитывать на заботливое и внимательное отношение.
Материал подготовлен по согласованию с врачом «Анадолу» терапевтом и медицинским онкологом Ешим Йилдырим.